Вы видите копию треда, сохраненную 23 февраля 2017 года.
Можете попробовать обновить страницу, чтобы увидеть актуальную версию.
Скачать тред: только с превью, с превью и прикрепленными файлами.
Второй вариант может долго скачиваться. Файлы будут только в живых или недавно утонувших тредах. Подробнее
Если вам полезен архив М.Двача, пожертвуйте на оплату сервера.



Третий пик - фанатка химии http://www.dailymail.co.uk/news/article-2059453/Heather-Raybon-disfigured-Illegal-meth-lab-explosion-caught-making-drug-again.html
Предыдущий тред >>362186 (OP)
https://www.youtube.com/watch?v=QmnrpjLJ7l8
Впрочем я сам накосячил, надо было греть до потемнения расплава, а не просто до плавления
Наука уровня /б/, хули.
Купил этилацетата в пэт - через 3-4 дней бутылка вздулась как барабан. От водорода, я думаю. Перелил в стекло.
При покупке меня предупреждали, что нужно сразу перелить из пэт.
Как твёрдая жёлтая капля
Разверни ПЭ, а то я вас дебилов знаю.
ПП - полипропилен? Мамой клянешься, что его ацетон/этилацетат не растворит?
Понимаю что платина, но всёже.
Какой биз можно открыть на основе знаний химии и небольшой лабы?
Кроме самогона и дуреварства
Нет, не бывает. Но у меня есть бутылки из ПП со вставками из ПЭВП со шкалой объема.
>>381604
ПА - полиамид
ПЭ - полиэтилен
ПЭТФ/ПЭТ - полиэтилен терефталат
ПП - полипропилен
ПЛ - полилактат
ПС - полистирол
Широко распространенные используемые обозначения, даже вика о них знает https://ru.wikipedia.org/wiki/Полиэтилен и https://ru.wikipedia.org/wiki/Полиэтилентерефталат
У меня прям сейчас уже который месяц ацетон стоит в этом, и ничего с бутылкой не случается.
В бизаче анон делал средства дезинфекции, потом получил лицензии и начал бюджетные деньги осваивать, а до тех пор - выживал, занимаясь грязной работой за копейки.
Мне для реакции
Покупал. Я не понимаю, как это меняет ситуацию. Кто-то азотную кислоту в пластик фасует, и че дальше?
>>381806
>ТГФ можно окислить марганцовкой?
1. Вы ебанулись про бутират на всех форумах писать? Вроде не было этого, и вдруг откуда-то целая толпа школьников, варящих бутираты.
2. Скорее всего получится янтарная кислота.
>Вы ебанулись про бутират на всех форумах писать?
Можно подумать лактон только для бутирата нужен
>Скорее всего получится янтарная кислота.
Чёт я сомневаюсь
>Можно подумать лактон только для бутирата нужен
А для чего еще? Нука придумай мне хотя бы еще одно применение.
>>Скорее всего получится янтарная кислота.
>Чёт я сомневаюсь
Я специально сейчас потратил целых пять минут на поиск ответа. Но тебе я его не скажу, потому что ты - сын шлюхи.
>>381825
>Можно визуально или на ощупь, кароч, без повреждений, отличить ПЭТ бутылку от ПЭ
Мне сложно представить, каким нужно быть всратым, чтобы спустать ПЭТФ с ПЭ. Ты можешь спутать стекло с парафином?
>каким нужно быть всратым, чтобы спустать ПЭТФ с ПЭ
Или я никогда не видел ПЭ бутылок, а только ПЭТ, но полиэтиленоввые пакеты похожи на ПЭТ бутылки. Или пакеты тоже ПЭТ?
Ну я на пробирках тоже не могу различить сорт стекла. Возьми что-нибудь потолще и побольше, хули ты. Как ты вообще собрался щупать какую-нибудь стрейч пленку, которая 40 мкм толщины, и ее толком не пощупаешь, потому что она вся тянется? Отмой скотч от клея и пощупай - неужели ты сможешь спутать это с пакетом из полиэтилена?
>>381838
"Братство Кольца", потом "Две крепости", потом "Возвращение короля".
>А для чего еще? Нука придумай мне хотя бы еще одно применение.
Прекрасный растворитель
>Но тебе я его не скажу, потому что ты - сын шлюхи.
Вот и за что мне такие беспочвенные оскорбления? Я даже не тот анон, который про марганцовку спрашивал. Уже и в дисскусию вступить нельзя
>Прекрасный растворитель
Вот, я не стал сразу говорить про абсурдность такого применения, чтобы ты смог обосраться. Ты же не будешь ебаться целый день для того, чтобы получить 100 мл прекрасного растворителя? С таким же успехом я могу сказать, что меткат - это прекрасный растворитель, для того я его у себя полкило и держу. А кетамином накипь в чайнике убираю. Все это было вполне резонно, пока за мое стремление к устранению накипи не стали давать более 10 лет.
Ну може тот кун гибкие солнечные батареи хочет сделать
Да да да ты тут самый умный никто не спорит(тут кроме нас двоих никого и нет)
Алсо волучится или винилацетат или кортоновая кислота, угадал?
получится быстрофикс
>"Братство Кольца", потом "Две крепости", потом "Возвращение короля".
Сам-то читал, советчик?
Прочитал тебе за щеку, проверяй
>Возьми что-нибудь потолще и побольше, хули ты.
Где я со 100% могу пощупать толстого ПЭ? Он же такой же прозрачный/бесцветный, как и ПЭТ?
Похоже по описанию на ПП - менее эластичный, чем ПЭ, глянцевый, более прочный.
Целулоид был сделан примерно для того же применения, что и ПЭТ, просто ПЭТ разработали позже примерно на 70 лет.
Крупы обычно фасуют в ПЭТФ. Целулоид был заменен на ацетилцелюлозу примерно в то же время, когда началось использование ПЭТФ, но сейчас уже и ацетилцелюлозу предпочитают не применять, а используют ПЭТФ. И прозрачные полипропиленовые пленки делают на ПЭТФ основе.
На полипропилене наносят рисунки, а ПЭТФ - в качестве опоры.
Кстати, двухсторонний скотч - это обычно ПП пленка.
Не где не читал об этом. Видать марганцовка слишком крутой окислитель для него или окисляет в янтарную кислоту. То же самое касается дихромата
Однако для селективного окисления в гбл применяют гипохлориты гипобромиты йодиты. То бишь хлорная известь или белизна
Кароч, я все равно не смогу отличить ПЭ бутылку от ПЭТ. Вполне может быть, что за всю жизнь я ни разу не видел ПЭ бутылки.
Эпоха ПЭТ.
У тебя, вполне возможно, есть судочки дома из ПЭ/ПП, можэешь еще зайти в строймагаз и посмотреть на бутылку акриловой грунтовки.
Решил получать "онлайн" прям перед экскрементом, чтобы знать кол-во и не морочить голову проблемой хранения. Окислил частично 40% спирт, и неилюзорно соснул хуйца, потому что в приемник капнула ровно одна капля. Оказывается, ебаный ацетальдегид прекрасно растворяется в воде и спирте, потому 10% раствор в 30% спирте кипит примерно при 60°C, то есть, ненамного раньше спирта (78,1°C) и намного выше чистого ацетальдегида (20°C). В этом плане он похож на формальдегид (но никак не малорастворимый в воде пропиональдегид), чего большинство мамкиных химиков почему-то не знает.
PS: вот вам еще смишняфка: "В настоящее время предприятие располагает мощностями по выпуску синтетических каучуков и продукции тонкой химической технологии и сложного органического синтеза: ацетальдегид, этилацетат, синтетический фенол и ацетон, метил-третбутиловый эфир, метилэтил-, метилвинилпиридин, а также продукции для использования внутри предприятия в качестве сырья". Почему-то вспомнился анекдот про советские микрокалькуляторы.
Нашел судочек из ПП - снизу указано PP
Мой вопрос про алканы, при каком n, добавление -СН2- не сильно меняет физические и химические свойства, т.е. образуется полимер (полиметан?)
Алканы вроде не полимеризируются.
>Я тебе не друг и я не спорил с тобой ни о чем
Чё блядь? Наркоман?
>Меньше нужно объебываться тиоцианатом.
Как ты узнал, сука? КАК БЛЯДЬ??

>>381838
Двачую.
Посоветуйте книги, учебники по химии, для разных уровней подготовленности.
Сейчас читаю пикрелейтед.
Например, в этой книге есть глава "Титрование с индикатором", в которой автор плавно переходит к обсуждению pH, в некотором смысле заходя на территорию Анатомии и, если угодно, Диетологии.
Но, ощущаю, что мне недостает некоторых структурированных знаний по химии.
В школе к химии относился халатно.
Теряюсь, когда автор употребляет такие обозначения и понятия как: "гидрокарбонат натрия", ионы, моли и т.п.
Цель: Просто люблю изучать жизнь.
Уровень подготовленности: Novice
"Начала химии" Кузьменко, Ерёмина и Попкова. Школьная программа по химии помещается в два маленьких тома.
Далее - "Неорганическая химия" Шрайвера и Эткинса или Хьюи (общие вопросы, связанные с неорганической и элементоорганической химией), "Неорганическая химия" Третьякова (химия элементов), "Современная органическая химия" Тернея и "Органическая химия" Реутова, Курца и Бутина. По аналитической химии - учебник Золотова.
Я щитаю что либо ты изучаешь химию и читаешь полноценные книги, либо читаешь научпоп.

Что нужно, чтобы провести эту реакцию и не сдохнуть/не убить соседей?
А зачем вам иприт, дяденька? ФСБ заинтересуется.
Надеюсь что не живу с тобой рядом.
Советую HO-CH2-CH2-Cl + Na2S, а потом кипячение с соляной кислотой.
Химзащита, раствор аммиака для дегазации
50 на 50. Быть специалистом - это всегда рандом. У меня папка стал инженеров, вот так же, как ты, и мамка стала, а потом они дружно, держась за ручку, соснули хуйца с развалом совка.
Очень удобно быть технологом-варщиком-прогером-тренером личностного роста.
Будет прям неебически вонять так, что полгорода в 04 звонить будут?
ПП может быть прозрачным как ПЭТ, менее эластичный, чем ПЭТ и это явно заметно. Жесткая хрень
ПЭ (правда я не знаю НД и ВД или еще какой) такой же эластичный, как и ПЭТ (руками разницу трудно ощутить, во всяком случае), но непрозрачный. Прозрачные только тонкие пленки.
Отреагируйте на меня, я щелочной металл
Рикомендую книжки брать отсюда.
в неорганику добавь Химию Элементов Гринвуда/Эрншо, в органику именные реакции Джей Джей Ли и ХГС Джоуля, в аналитику АХ Кристиана и АХ Кельнера, по физхимии Эткинс

>Это вообще реально?
Нет. Можно дохуя разбираться в органике, но вдруг эксперимет может показать, что ты нихуя не разбираешься
Механизмы органических реакций Сайкса, можно ещё Реутова навернуть или Кэри/Марча, но новые издания на ингрише

>Сайкса
Почитал, какой-то лютый пиздец. Сначала пишет что в теории вот так, потом пишет что на деле есть исключение и на самом деле речь идет про математическую модель.
помоему в химии так часто бывает? в общей, не знаю про органику.
в физике так-же. механика, которая не применима к малым телам или геометрическая модель света.
>не знаю про органику
Речь как раз про органику. Это какой-то очень упоротый химический матан с энергией орбиталей и связей. Это конечно то что я просил, но онписано очень черезжопно и в каждом параграфе есть примеры которые противоречат теории.
1.Взял 18650 аккум.
2.Посадил его в ноль.
3.Разобрал и кинул потроха в воду.
По идее оксид лития должен перейти в гидроксид с образованием кислорода и раствориться в воде.
4.Фильтрую. Получаю гидроксид лития растворенный в воде.
5.Сушу и получаю оксид.
6.Прокаливаю и получаю карбонат.
Все верно?
Интересно как ты получишь карбонат обычным прокаливанием ? Если ты конечно забыл упомянуть что в углекислой среде.
Смотря в какой атмосфере. Ты походу двачуешь с Венеры, в атмосфере которой 96,5 % CO2. У нас же на Земле такое не получится.
>>383642
Если не перегревать то вполне можно. Но даже так учитывая что углекислота тяжелее кислорода ничего сложного не вижу, уксусная кислота и сода идут на помощь.
Подтвержу слова анона выше про то, что сами химики до конца не понимают реакции, а иногда и с самого начала не понимают.
Я приведу вам очень простой пример, сейчас весь состав химиков пойдет резать вены от осознания своей ничтожности и некомпетентности.
Итак: почему NaCl растворяется в воде, но не растворяется в изопропаноле?
Isopropyl alcohol:
Molecular weight 60.10
Melting point in °C -90
Boiling point in °C82
Density in g/cm 3 at 20 °C 0.7855
Electric dipole moment in debye units 1.56
Water:
MW 18.02
boiling point (°C) 100.00
melting point (°C) 0.00
density (g/mL) 0.998
Dielectric Constant (D) 1.8546
Люблю долбоебов, которые как заведенные повторяют "дихлорметан - неполярный растворитель". Извините меня, тогда вода - тоже неполярный растворитель, какие-то ссаные 1.85 D против против 2,69 D у ацетона.
Пардон, последнее, конечно же, не диэлектрическая константа, которая в дебаях не измеряется, а дипольный момент.
> вода - тоже неполярный растворитель
Здрасте нате. С чего это вода неполярный растворитель когда у неё поляризация в сторону 2х молекул водорода идет?
Не отгадал. Спирты тоже поляризованы, спирты тоже являются протонными растворителями, и pKa у них близкий к воде. Таким образом, у них по этим критериям должна быть почти такая же растворимость NaCl, ну может чу-уточку меньше.
>>383678
https://ru.wikipedia.org/wiki/Полярные_вещества
"Полярные вещества в химии — соединения, молекулы которых обладают электрическим дипольным моментом"
Я привел значения дипольных моментов. В случае дихлорметана дипольный момент равен 1,62 https://en.wikipedia.org/wiki/Dichloromethane_(data_page) , то есть, в общем-то, дихлорметан - это полярный апротонный растворитель.
Так блять ты уже определись изопропанол или дихлорэтан. У тебя каша какая-то ебаная в постах и в голове.
Я вполне раздельно пишу, и я написал разные дипольные моменты для дихлорметана и для изопропанола, и про дихлорметан я отвечал только на дихлорметановое обсуждение, так что каша - только у тебя в голове.
Ты понимаешь что ты наркоман?
>Итак: почему NaCl растворяется в воде, но не растворяется в изопропаноле?
>Люблю долбоебов, которые как заведенные повторяют "дихлорметан - неполярный растворитель". Извините меня, тогда вода - тоже неполярный растворитель
Я понимаю, что у тебя погорело, но это тебя не оправдывает. Тебя удивляет, что я отклонился от священых писаний, но я настаиваю на том, что в ваших писаниях написана ересь.
Историю с дихлорметаном я упомянул, потому что она имела место в жизни, ведь найдется довольно немало людей. которые скажут, что дихлорметан - неполярный растворитель, хотя эта класификация некоректна в свете того, что полярность у дихлорметана почти такая же, как у воды.
Здесь вопрос стоит в том, а нужна ли вообще такая класифкация? С подобным успехом можно делать растворители на кошерные и некошерные - давайте и это тоже писать в учебниках. А че, толку столько же.
(Автор этого поста был забанен. Помянем.)
Ты еще спроси почему для решения школьных задач по геометрии нельзя интеграл брать. Примеры у тебя наркоманские, я их логику уловить не могут, сначала про ерему потому про фому, у меня от этого пригорело. Ересь какую-то написал, вода у не полярный растворитель. И вообще если есть смещение поляризации значит уже полярный растворитель, диполный момент и всякое такое это уже лютая теория которая абсолютно не всегда вписывается в практику. Как говорил Эйнштейн "если теория не может правильно описать практику значит теория должна изменится", только и всего.
Какое такое смещение поляризации? Ты давай мне не путай фиксированный диполь (полярность) с индуцируемым диполем (поляризуемость), потому что как раз у хорошо поляризуемых молекул фиксированный диполь маленький или отсутствует вовсе.
Полярность, поляризуемость, диссоциация - это физические свойства растворителей, которые можно объективно измерить.
Однако, от этого школьно-институтская залупонь не перестает сосать хуйцов, ведь практически никто из них не может объяснить "парадокса растворимости соли", хотя ответ до безобразия прост.

А ты тоже поломай голову, почему резорцин хорошо растворим в воде, а фенол умеренно растворим в воде.
Сейчас он прозреет, как до мезомерного эффекта дойдёт и заместителей электроно-доноров электроно-акцепторов и их влияние на химические и физические свойства.
не химик.
в спирте, O поляризует C, С поляризует два других карбона. тем самым уменьшая конецентрацию положительного заряда на C-O карбоне, распределяя заряд на все карбоны. то-есть атомы карбона не поляризуются сильно. поляризуется O-H и возможно не так сильно как у воды. нужно смотреть на electron density model, но я не нашел.
молекула воды меньше молекулы спирта. на площадь NaCl можно разместить больше молекул воды, чем молекул спирта.
goatse
Подскажи мне что-то очень вонючее и не смертельное. Мне приходят на ум только не очень гуманные и сложные синтезы с образование газообразного хлора, акролеин и тому подобные хлорацетоны.
На самом деле пахнет, просто ты не так сильно ощущаещ запах именно своего, типа привык к своему запаху.
Какова вероятность что среди алкашей будет профессиональный сомелье способный вычислить меня по запаху говна?
Ну а вдруг. Короче надо не такой палевный способ.
Дипольный момент - это интегральная оценка всех молекул вещества. То, что углеводородный хвост оказывает влияние на дипольный момент, отражено в величине дипольного момента - она ниже примерно на 10% у спирта и хлороформа чем у воды.
Если книга, которую ты цитируешь, была написана до 1950 года, то, в принципе, автора еще можно оправдать. Уже в 1940 в научной среде все заинтересованные знали обо всех известных сейчас механизмах, влияющих на растворимость, и после 1950 года не было никакого иного объяснения для того чтобы упускать эти факты, кроме того, что автор - мудак.
Запощеная тобой пикча только вскользь упоминает факторы, которые могу относиться к вопросу растворимость соли в изопропаноле и воде.
>>383697
>Ладно бы нормально троллил, но ведь хуйню пишет путаясь в номенклатуре.
Что, пригорело так сильно от своей некомпетентности, что тебе даже приходится придираться к моей нуменклатуре? Хотя, я не помню, когда это я в ней запутался. Дипольный момент-диэлектрическая константа, что ли?
>>383698
>А ты тоже поломай голову, почему резорцин хорошо растворим в воде, а фенол умеренно растворим в воде.
Водородные связи. Несмотря на снижения дипольного момента гидрохинона и пока что не скажу чего, у гидрохинона растворимость почти такая же, как у фенола. Потому что есть водородные связи, которые у гидрохинона, пирокатехола, и резорцинола сильнее, чем у фенола. Почему-то у резорцинола роль водородных связей заметнее, чем у пирокатехола, по ряду вода-спирт-хлороформ-бензол это заметно, ни что иное, нежели водородные связи, конкретно в этом вопросе влияния не оказывают.
Вот я вам выдал нагора один из ключевых факторов, окай, разница в 10 раз стала ясна, теперь дело за малым - объяснить разницу еще в 300-1000 раз.
>>383699
Я сомневаюсь, что эти факторы в вопросе фенол-резорцинол-гидрохинон-пирокатехол играют важную роль, хотя, абсолютно точно, какую-то лепту вносят. Все же, мне кажется, что экранирование водородный свяхей в пирокатехоле по сравнению с резорцинолом куда более значимо, чем снижение pKa на 0.3-0.6 из-за заместителя.
Дипольный момент - это интегральная оценка всех молекул вещества. То, что углеводородный хвост оказывает влияние на дипольный момент, отражено в величине дипольного момента - она ниже примерно на 10% у спирта и хлороформа чем у воды.
Если книга, которую ты цитируешь, была написана до 1950 года, то, в принципе, автора еще можно оправдать. Уже в 1940 в научной среде все заинтересованные знали обо всех известных сейчас механизмах, влияющих на растворимость, и после 1950 года не было никакого иного объяснения для того чтобы упускать эти факты, кроме того, что автор - мудак.
Запощеная тобой пикча только вскользь упоминает факторы, которые могу относиться к вопросу растворимость соли в изопропаноле и воде.
>>383697
>Ладно бы нормально троллил, но ведь хуйню пишет путаясь в номенклатуре.
Что, пригорело так сильно от своей некомпетентности, что тебе даже приходится придираться к моей нуменклатуре? Хотя, я не помню, когда это я в ней запутался. Дипольный момент-диэлектрическая константа, что ли?
>>383698
>А ты тоже поломай голову, почему резорцин хорошо растворим в воде, а фенол умеренно растворим в воде.
Водородные связи. Несмотря на снижения дипольного момента гидрохинона и пока что не скажу чего, у гидрохинона растворимость почти такая же, как у фенола. Потому что есть водородные связи, которые у гидрохинона, пирокатехола, и резорцинола сильнее, чем у фенола. Почему-то у резорцинола роль водородных связей заметнее, чем у пирокатехола, по ряду вода-спирт-хлороформ-бензол это заметно, ни что иное, нежели водородные связи, конкретно в этом вопросе влияния не оказывают.
Вот я вам выдал нагора один из ключевых факторов, окай, разница в 10 раз стала ясна, теперь дело за малым - объяснить разницу еще в 300-1000 раз.
>>383699
Я сомневаюсь, что эти факторы в вопросе фенол-резорцинол-гидрохинон-пирокатехол играют важную роль, хотя, абсолютно точно, какую-то лепту вносят. Все же, мне кажется, что экранирование водородный свяхей в пирокатехоле по сравнению с резорцинолом куда более значимо, чем снижение pKa на 0.3-0.6 из-за заместителя.
1,2- Dihydroxybenzene 2.62 ±0:03
1.3- Dihydroxybenzene 2.07 ±0.02
1 ,4-Dihydroxybenzene 1.4
Дело в том, что он растворяется хуже, чем фенол, во всех растворителях:
- в бензоле для фенола 10 г/100мл против гидрохинона 0.03 г/100 мл;
- в воде 8 г/100мл фенол и 7.33г/100мл гидрохинон;
- фенол в глицерине 276,4 гТ
Для фенола logP = 1.46, для гидрохинона logP = 0.59 (0.46 по другим сведениям), пирокатехол logP = 1.04, резорцинол logP=0.62.
Такое ощущение, что его симетричная структура за счет усиления взаимодействия молекул гидрохинона друг с другому приводит не только к увеличению температуры плавления (172°C у гидрохинона против 40.5°C у фенола), но и к снижению растворимости.
...
- фенол в глицерине 27,6 г/100мл
- гидрохинон в метаноле, 33.7 г/100мл;
- гидрохинон в этаноле 33 г/100мл (не знаю, насколько оправдано это сравнение).
>Запощеная тобой пикча только вскользь упоминает факторы, которые могу относиться к вопросу растворимость соли в изопропаноле и воде.
Абсолютный шизик, противоречишь сам себе.
>Что, пригорело так сильно от своей некомпетентности.
Я не этот анон, но выше ты путаешь изопропанол и дихлорметан.
>Водородные связи. Несмотря на снижения дипольного момента гидрохинона и пока что не скажу чего, у гидрохинона растворимость почти такая же, как у фенола. Потому что есть водородные связи, которые у гидрохинона, пирокатехола, и резорцинола сильнее, чем у фенола.
>Почему-то у резорцинола роль водородных связей заметнее, чем у пирокатехола
Вот тут ты и попался. Ты нагуглил какую-то статью, но если бы ты получил хотя бы школьное образование ты сразу знал без всяких почему-то. Наводящие вопросы гидроксигруппа электронодонор или электроноакцептор? Как плияют орто- мета и пара- положения заместителей на реакционную способность молекул? Как идёт растворение в полярных растворителях, именно основной механизм, а то сейчас опять свои шизоидные дипольные моменты найдёшь.
>Все же, мне кажется, что экранирование водородный свяхей в пирокатехоле по сравнению с резорцинолом куда более значимо, чем снижение pKa на 0.3-0.6 из-за заместителя.
Опять полное незнание и неграмотность. Что такое pKa? 0,3-0,6 это типа так мало? А теперь сравни реальные концентрации ионов водорода, без показателя. Там будет разброс на порядки.
Шизик это ты:
- ты говоришь мне про статью, но ты не можешь ее нагуглить, потому такой статьи нигде нет и не было - это мои собственные выводы (которые можно обосрать, потому что есть некоторые неточности);
- ты путаешь дихлорметан с изопропанолом, но обвиняешь в этом меня.
>Как плияют орто- мета и пара- положения заместителей на реакционную способность молекул?
- я уже ответил частично.
>0,3-0,6 это типа так мало?
Да, это очень мало, это увеличение концентрации протонов в 1.16-1.35 раз - сильно меньше, чем наблюдаемое отношение растворимостей в 10 000 раз.
Чудненько, мы будет обсирать оппонента и до последнего пытаться защитить свои давным-давно опровергнутые аргументы, нежели искать ответ. Как грица, есть знания - нет понимания.
Вот правильный ответ
https://en.wikipedia.org/wiki/London_dispersion_force
https://en.wikipedia.org/wiki/Intermolecular_force#Relative_strength_of_forces
Собственно, причина, по которой соль не растворяется в воде, та же, почему октанол не растворяется в воде.
А ты сам читал ссылку, которую я привел? Так может по сути отвечать будешь? Или мне тебе еще нужно объяснить, каким образом силы межмолекулярного взаимодействия относятся к растворимости?
Это шизик, он теперь пишет вот почему октанол не растворяется в воде. Хотя в начале беседы было про натрия хлорид и изопропанол вот пруф >>383675 , вообще репортим мочератору чтобы поехавшего забанили
>>384285
Изонитрил же, только смертельный он. Но надышаться до смерти не получится.
>>384408
>это мои собственные выводы (которые можно обосрать, потому что есть некоторые неточности)
Ты же гений у нас куда там до тебя Менделеву с его таблицей, да и нам болезным.
>Да, это очень мало, это увеличение концентрации протонов в 1.16-1.35 раз - сильно меньше, чем наблюдаемое отношение растворимостей в 10 000 раз.
Да что ты говоришь, иди-ка посчитай, ебаный школьник, изменение pKa c 2.7 до 2.03, т.е. на 0.67 приводит к увеличению концентрации ионов водорода в 4,6773 раза, т.е. почти 500%. И ещё раз повторяю, дипольный момент и показатель константы диссоциации кислоты, ни капли не влияют на растворимость и растворение, хотя бы потому что механизмы растворения различных веществ в полярных и неполярных растворителях отличаются друг от друга.
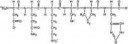
>Или мне тебе еще нужно объяснить, каким образом силы межмолекулярного взаимодействия относятся к растворимости?
Ок, тогда по твоему этот полипептид будет неограниченно смешиваться с водой, спиртами и т.д. У него же слабое межмолекулярное взаимодействие, так?
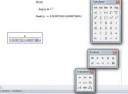
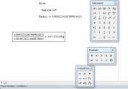
Вот отклеились пики где шизик обсирается с расчётами по pKa, ну и где тут 1.16-1.6 раза?
>иди-ка посчитай, ебаный школьник, изменение pKa c 2.7 до 2.03, т.е. на 0.67 приводит к увеличению концентрации ионов водорода в 4,6773 раза, т.е. почти 500%
У меня есть стойкое ощущение, что ты - это все тот же долбоеб, который мне пишет, что я чего-то не понимаю, хотя только он один в это время не понимает.
https://en.wikipedia.org/wiki/Acid_dissociation_constant
Ka = [A-][H+] / [HA]
Поскольку Ka сильно меньше единицы (pKa >> 0), то [HA] примерно постоянно. При условии отсутствия заметного влияния щелочи или кислоты, [A-] = [H+], как ионы одной и той же молекулы. Отсюда
Ka = [H+]^2 / [HA]
[H+] = sqrt(Ka*[HA])
или в логарифмах
pH = (pKa + log[HA])/2
Изменение pKa на 0.67 приводит к изменению pH на 0.67/2 0.335, или, возводя в степень 10, 2.16 раз.
Вот папка тебя и научил химии. К сожалению, матлаб химии не учит, потому что сам ее не знает. Может когда-нибудь ты еще узнаешь, что находить аргумент интеграла можно просто возводя в степень, как-нибудь в следующий раз поучимся.
>>384430
Амидную цепь без значимого диполя можно считать гидрофильной (водородные связи). Здесь 2 карбоксильные, 3 аминовые, 1 тиольная група, и еще солидная кучка гидрофобных груп. Итого, кислотных и основных груп довольно много, но они заземлены сами на себя (понижение растворимости с сохранением гидрофильности), плюс гидрофильный амид, а им противостоят гидрофобные групы - где-то 8 г на 100 мл растворится я думаю получится (брал тупо по растворимостям гистидина, глутамина, и аспарагиновой кислоты помножить на 2). В этаноле, и тем более в апротоных растворителях, из-за двух внутримолекулярных ионых связей растворимость еще ниже (да, эта молекула гидрофильна!). Замени все свободные амины на карбоксилы - получится на порядок более растворимое соединение, и в воде, и в спирте, и в апротоных растворителях. Докинь щелочи - ни в чем, кроме воды и каких-нибудь ионых жидкостей, оно не будет растворяться.
>будет неограниченно смешиваться с водой, спиртами и т.д. У него же слабое межмолекулярное взаимодействие, так?
У него весьма большое значение лондоновской дисперсии. Если повыкидывать цистеин, лизин, гистидин, бета-аминоксилоту, то ничего не останется получится вполне яркая гидрофильная молекула с растворимостью в воде >30 г/100мл. С каждой углеводородной групой размер молекулы растет, дисперсионые силы увеличиваются, а влияние функциональных груп снижается, потому что им приходится тянуть за собой хвост. А, как я уже несколько раз сказал, гидрофильные функциональные групы замкнуты сами на себя, потому тащить у них получается хреново.
Тут еще есть такая хуйня, как повышение температуры, там что-то веселое может нарисоваться, типа повышения растворимости в воде.
>иди-ка посчитай, ебаный школьник, изменение pKa c 2.7 до 2.03, т.е. на 0.67 приводит к увеличению концентрации ионов водорода в 4,6773 раза, т.е. почти 500%
У меня есть стойкое ощущение, что ты - это все тот же долбоеб, который мне пишет, что я чего-то не понимаю, хотя только он один в это время не понимает.
https://en.wikipedia.org/wiki/Acid_dissociation_constant
Ka = [A-][H+] / [HA]
Поскольку Ka сильно меньше единицы (pKa >> 0), то [HA] примерно постоянно. При условии отсутствия заметного влияния щелочи или кислоты, [A-] = [H+], как ионы одной и той же молекулы. Отсюда
Ka = [H+]^2 / [HA]
[H+] = sqrt(Ka*[HA])
или в логарифмах
pH = (pKa + log[HA])/2
Изменение pKa на 0.67 приводит к изменению pH на 0.67/2 0.335, или, возводя в степень 10, 2.16 раз.
Вот папка тебя и научил химии. К сожалению, матлаб химии не учит, потому что сам ее не знает. Может когда-нибудь ты еще узнаешь, что находить аргумент интеграла можно просто возводя в степень, как-нибудь в следующий раз поучимся.
>>384430
Амидную цепь без значимого диполя можно считать гидрофильной (водородные связи). Здесь 2 карбоксильные, 3 аминовые, 1 тиольная група, и еще солидная кучка гидрофобных груп. Итого, кислотных и основных груп довольно много, но они заземлены сами на себя (понижение растворимости с сохранением гидрофильности), плюс гидрофильный амид, а им противостоят гидрофобные групы - где-то 8 г на 100 мл растворится я думаю получится (брал тупо по растворимостям гистидина, глутамина, и аспарагиновой кислоты помножить на 2). В этаноле, и тем более в апротоных растворителях, из-за двух внутримолекулярных ионых связей растворимость еще ниже (да, эта молекула гидрофильна!). Замени все свободные амины на карбоксилы - получится на порядок более растворимое соединение, и в воде, и в спирте, и в апротоных растворителях. Докинь щелочи - ни в чем, кроме воды и каких-нибудь ионых жидкостей, оно не будет растворяться.
>будет неограниченно смешиваться с водой, спиртами и т.д. У него же слабое межмолекулярное взаимодействие, так?
У него весьма большое значение лондоновской дисперсии. Если повыкидывать цистеин, лизин, гистидин, бета-аминоксилоту, то ничего не останется получится вполне яркая гидрофильная молекула с растворимостью в воде >30 г/100мл. С каждой углеводородной групой размер молекулы растет, дисперсионые силы увеличиваются, а влияние функциональных груп снижается, потому что им приходится тянуть за собой хвост. А, как я уже несколько раз сказал, гидрофильные функциональные групы замкнуты сами на себя, потому тащить у них получается хреново.
Тут еще есть такая хуйня, как повышение температуры, там что-то веселое может нарисоваться, типа повышения растворимости в воде.
>Или мне тебе еще нужно объяснить, каким образом силы межмолекулярного взаимодействия относятся к растворимости?
Объясняй.
Притягивающиеся молекулы стремятся тусить вместе, не притягивающиеся - порознь. Все просто, как у людей. Если ты суешь апротоно-дисперсионого неформала в толпу крайних протоно-настроенных аборигенов, то они его вытолкнут немедленно.
Хлорид натрия слабо притягивается к спирту. Чем больше хвост, тем хуже притягивается, и тем плотнее спирт в тусовке неформалов (лондонских).
Хвост, по отношению с биполярными эквивалентностями смешивается с дихлорметаном, так вот, для полного растворения, этого самого изопрапанола должно быть в два раза больше.
>У него весьма большое значение лондоновской дисперсии. Если повыкидывать цистеин, лизин, гистидин, бета-аминоксилоту, то ничего не останется получится вполне яркая гидрофильная молекула с растворимостью в воде >30 г/100мл. С каждой углеводородной групой размер молекулы растет, дисперсионые силы увеличиваются, а влияние функциональных груп снижается, потому что им приходится тянуть за собой хвост. А, как я уже несколько раз сказал, гидрофильные функциональные групы замкнуты сами на себя, потому тащить у них получается хреново. Тут еще есть такая хуйня, как повышение температуры, там что-то веселое может нарисоваться, типа повышения растворимости в воде.
А теперь отсоси мой член, падла, этот полипептид нерастворим в воде, совсем, он образует КОЛЛОИДНЫЙ раствор и относится к ограниченно набухающим коллоидом.
Белки все таки набухают в воде. Имеет место быть гидрофильное взаимодействие. А теперь сделай то же самое с битумом. Хуй там плавал
Вобще тут сброд какой то. Даже в учебнике глинки написано, что точно предсказать растворимость веществ в друг друге не возможно. Есть конечно теории, пресказыващие это, но со 100% вероятностью не скажешь
Как начет повариться мяско в расплавленой щелочи?
>Вобще тут сброд какой то. Даже в учебнике глинки написано, что точно предсказать растворимость веществ в друг друге не возможно. Есть конечно теории, пресказыващие это, но со 100% вероятностью не скажешь
Почитай внимательнее: этот поехавший "разработал" свою теорию, однако его тут обоссали.
Ну я тоже конечно неправ, я показал этому школьнику только кусочек, на самом деле эти цвиттер-ионы сами по себе скручиваются в глобулы, этим и объясняется образование коллоидного раствора.
>так вот, для полного растворения, этого самого изопрапанола должно быть в два раза больше.
Почему же?

Высота - 4,5 см.
Ширина в верхней части - 4см.
Мягкий металл (руками можно сжать), по цвету похож на нечто среднее между хромом и аллюминием.
По верхнему ободку маркировка - то ли PtB то ли Pt5
Это ни тигель вероятнее всего, это свинцовый стакан для чего-то радиоактивного. Если так то зря ты его вообще взял, непонятно что в нем было и он может быть загрязнен чем-нибудь и фонить. Если есть хороший дозиметр с раздельной бетой и гаммой то проверь лучше.
Он без крышки и тонковат для хранения радиоактивного. У свинца есть какие-нибудь характерные особенности?
Ногтем не царапается, острый нож оставляет царапину. Может, олово?

Сорь за качество. Выгладит как пикрил. Если будет возможность - сфоткаю
Сходи в ломбард, там тебе взвесят до сотых. Вангую у тебя платиновый тигль в руках.
Посмотрел тут креосана и захотелось мне корбида.
Я так понял что можно взять известь, смешать с углем и хорошенько нагреть. Все правильно? До скольки надо греть?
2000
Смотря что и смотря где.
>порвался
Что? Я не порвался. Так из ацетилена много разных веществ можно синтезировать? И это есть в этой книге? Если да то я тоже почитаю.
Но я не шутил. Я действительно не понимал что это такое. Ну знаю карбиды, но вот корбид нет. Но теперь мне ответили и я понял что корбид это карбид кальция.
Я покупал как частное лицо.
Из ацетилена можно синтезировать прекурсоры и собственно вещества, да и бытовом плане вещь очень полезная, я с помощью ацетилена ускорял дозревание томатов.
Где бы почитать про это все? Особенно про томаты.
для синтеза бутандиола из ацетилена нужно давление 10 атм и катализаторы. Плоховй вариант
>можно синтезировать
>можно
Из много чего МОЖНО синтезировать прекурсоры. Вопрос только в адекватности реакции те возможности завернуть ласты и её эффективности те полезном выходе задуманного вещества. Я читаю такие МОЖНО и ахуеваю. МОЖНО себе хуй в жопу засунуть, и ебать себя в сраку.
Бьют по шее максимум.

Стало интересно, как же выделить чистое золото?..
Вот, нашёл, значит: азотная кислота не растворяет золото и платиновые металлы,
но растворяет серебро и другие металлы и их оксиды. Золото и платина - выпадают при этом, в виде осадка.
Царская водка растворяет золото и платину, а серебро - падает в осадок.
А вот золото от платиновых металлов отделить можно при электролитическом рафинировании золота.
Если применять в качестве электролита разведенную теплую соляную кислоту,
то золото растворяется на аноде, состоящем из сырого золота вместе с платиновыми металлами. А на катоде же выделяется только золото, в то время, как последние могут накопляться в растворе в виде комплексных ионов.
Парочку реакций, сюда бы:
1. Царская водка.
3HCl + HNO3 = 2Cl↑ + NOCl + 2H2O, где NOCl - хлорид нитрозила.
2. Раствор золота в царской водке.
Au + HNO3 + 4HCl = HAuCl4 + NO↑ + 2 H2O,
где H[AuCl4] - растворимый тетрахлороаурат водорода.
3. Восстановление золота из раствора тетрахлороаурата водорода - железным купоросом:
H[AuCl4] + FeSO4 = Au↓ + Fe2(SO4)3 + FeCl3 + HCl
Да, и вот ещё:
азотная кислота - HNO3;
золото - Au;
серебро - Ag;
платиновые металлы - Ru, Rh, Pd, Os, Ir, Pt;
железный купорос - FeSO4.
>Если применять в качестве электролита разведенную теплую соляную кислоту
Тут процесс сложнее, чем (Au + HCl)
Потому что, вот так вот: Au + 4Сl⁻ -3е → АuCl⁻4
Поэтому, оставлю это здесь.
http://znaesh-kak.com/au/zoloto/rafinirovanie_zolota.html
>из минералов
>можно получать
>любые металлы
>c помощью электролиза
>и кислот
>в
>оксид
>добавить хлоридную кислоту
>соли расплавить
>и электроиз
Ну, во-первых, не все металлы и их оксиды взаимодействуют с HCl;
во-вторых, нельзя просто так взять и расплавить все соли;
в-третьих, как ты потом выделять собрался отдельные металлы из их сплава, что на катоде - в результате электролиза расплава кучи этих всяких разных солей?..
Низя. Химия не математика, здесь нет четких формул типа х+у=z.
Я прост ни разу не видел в русскоязычных учебниках таблицы эл потенциалов. Только в муррикнаских.
Это что? Можно подобрать напряжение при котором ион одного (с самым меньшим нужным напряжением) элемента будет образовываться на электроде?
>>385644
Это количество энергии которое можно получить при реакции. Чем больше тем более экзотермичная, чем меньше тем эндотермичная.
Таблица стандартных ЭЛЕКТРОДНЫХ ПОТЕНЦИАЛОВ, же. Ещё и в водной среде.
>>385644
Ну представь, что у тебя раствор содержит все ионы вместе взятые.
Регулируя напряжение на электродах, ты можешь воздействовать с помощью электродов на определённые, конкретные ионы, из этого раствора.
А если это расплав солей, и металлы выделяются на катоде, то как-бы
сменой электродов и подключения их к разным напряжениям, как-бы можно-таки получить разные катоды с осаждёнными на них различными металлами из всей этой каши-малаши.

В сосничестве я был настолько ленив, что вечером и ночью не ходил в сортир, а просто ссал на стены рядом с кроватью. Обои тогда хорошо пропитались, и даже спустя много лет от них знатно шмонит, особенно в тёплое время года.
Сейчас взялся за переклейку обоев во всей комнате, ободрал старые, но в тех местах, которые я обоссывал, потёки мочи и вонь присутствуют даже на голых стенах.
Механические способы удаления типа наждачной бумаги не подходят, ибо гипсокартон. Так что остаются только химические.
Чем очищать вонявые стены, аноны?
Содой.
Сожги нахер эти стены.
Карбамид (мочевина, диамид угольной кислоты) температура разложения - 150-160° C'
Какой же ты конченый. Можно попробовать хлорку или окислительль какой. Пергридоль там
Да ладно? У того же Третьякова были диаграммы Латимера.
Ребят, поступил на первый курс на специальность, тесно связанную с химией. В школе благополучно пропустил почти весь курс(знаний крайне мало), так как и желания не было(нафиг мне какие-то формулы, хы хы хы, так на уроках и сидел), да и учитель был крайне плох и забивал на наш класс болтяру. А вот сейчас и учить её придется, да и самому очень интересно начать изучение этой прекрасной науки. В общем, что посоветуете для начала?
В детстве был ленив
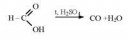
CO - ядовит.
Пролистай тред, где-то в самом начале советовали учебники для самообразования, но для начала лучше прочти школьные учебники чтобы хотя бы было базовое понимание и знание/понимание основных терминов.
Все заебок, но спирт вероятно гидролизный непочищеный. И по мимо муравьинки там дохера говна
Правильно боишься. Вылей эту срань.
Спасибо, идея про школьную литературу звучит неплохо, но сам я думал что там много воды. Попробую, посмотрим что выйдет
Вряд ли будет только химия. Заканчиваю учиться на химика/инженер-технолога по специальности физика-химия тугоплавких неметалических и силикатных материалов в КНИТУ-КХТИ. У меня были нехимические предметы: Математика, информатика, иностранный(у меня был английский, но у некоторых немецкий) язык, у заочников был русский язык(!), история россии, физика, физ-ра, вычислительная математика, прикладная механика(сопромат), История и культура Татарстана(хотя я из Башкирии, и мне нахуй это не надо), Программно-технические комплексы(Инженерная графика, но только на компе), философия, ЭиПЭ(электротехника), Техническая термодинамика и теплотехника, Введение в предпринимательство, Основы экономики и управление предприятием, социальная организация, правовединие, основы маркетинга, БЖД, Экология, Общезаводское хозяйство предприятий, спецификация и стандартизация технологии неорганических веществ, автоматизации, основы химической технологии(ОХТ), тепловые процессы и аппараты технологии тугоплавких неметалических и силикатных материалов(печи и сушилки всякие), ПАХТ(Приборы и аппараты химической технологии), химические реакторы и т.д. Из химии: неорганическая химия, органическая химия, коллоидная химия, аналитическая химия, физико-химические методы анализа, физическая химия, материаловедение и защита от коррозии, РСХС(реакционная способность химических соединений), Минералогия и Кристаллография, твердофазные реакции, компьютерная химия, основы технологии тугоплавких неметаллических и силикатных материалов, Физико-химия технологии тугоплавких неметаллических и силикатных материалов и т.д.
Кароче можешь особо не залегать, школьных знаний достаточно, остальное тебе разжуют преподаватели и практика в лаборатории, если интересно можешь заняться самообразованием.
>>386171-кун
Не читай советское говно, лучше вообще никогда не трогай ничего советского, это лютый пиздец.
Почему нанотрубок и фуллеренов нет на фазовой диаграмме p-T углерода?
Я понимаю, но просто в остальных предметах я разбираюсь более-менее, а вот с химией полный пиздец
Там же - перегонный куб.
Этанол/Температура кипения - 78,37°C
Муравьиная кислота/Температура кипения - 100,8°C
Разница температур маловата для простой перегонки. Попробуй связать муравьиную кислоту содой.

Муравьиная кислота же с этанолом реагирует - образуя пропионовую кислоту. Температура кипения - 141 °C
температура вспышки - 54 °C.
HCOOH + C2H5OH -> С2Н5-СООН + H2O;
Только реакция идёт при наличии концентрированной серной кислоты, как водоотнимающего средства.
Температура кипения серной кислоты - 337°C.
H2SO4 + H2O -> H3O+ + HSO4-;
И так как муравьиный спирт - 1,4 % раствор муравьиной кислоты в 70 % этаноле, реже в 96 % спирте, считаешь количество кислоты в молях и гасишь ею воду, с последующей перегонкой в кубе.

>Температура кипения серной кислоты - 337°C.
Гугл лагает.
или википедия?..
Т. плав.10,38 °C
Т. кип.279,6 °C
И да, она же и без кипения, может испаряться, не?..
Так что, соды не забудь.
Качаешь рабочую программу с сайта министерства образования, сморишь книги и пиздуешь в библиотеку, либо на какой-нибудь трекер.
Только для проработки - нужны задачи и примеры.
>И так как муравьиный спирт - 1,4 % раствор муравьиной кислоты в 70 % этаноле, реже в 96 % спирте, считаешь количество кислоты в молях и гасишь ею воду, с последующей перегонкой в кубе.
>
Что?
Это что за неведаная реакция такая? Как называется?
Сука блядь. Соды туда заебаш
Все нормально, у нас тут химия уровня /б/. И я бы даже не сказал что это плохо, химия она такая, в нельзя просто делать как написано. Потому что вдруг написана хуйня? Но я бы все ровно не стал пить эту срань.
>>386159
Чистота проверяется просто. Берешь стекляшку, берешь [/s]свой хуй в руку[/s] пипетку и капаешь капельку на стекло. Если спирт испарился и осталась хуйебень то все плохо. Но так или иначе знай что надо 6 перегонок чтобы получить из браги 96% спирт. Так что если ты заморочишься и замутишь много перегонок есть шанс не попротить здоровье. Но пить бы это я бы все ровно не стал.
>браги
Какой браги епт, если тот идиот занимается какой-то хуйней с аптечными пузырями, вместо того, чтобы купить мешок сахара и пачку дрожжей.
>>386359
Ну охуеть теперь, разница температур мала. Все самогонщики сейчас осознали, какой же глупостью они занимаются, ведь температура кипения воды еще ниже.
ааааааааааааааааааааааааааахахха.
Что за пиздежь? Поступил на химию, ни по химии, ни по матану никаких основ не рассказывают - сразу с места в карьер хуета в духе "А вот это ж вы уже знаете, так что решим вот эти задачки".
Я такой - О__о , так как школу кончал несколько лет назад, нихера не помню, а егэ не сдавал. Охуеть.
Возможно ли вещество у которого отсутствует полиморфизм? Например у углерода до хрена этих полиморфных модификаций, а если вещество у которого только одна модификация и она постоянна при любой температуре, давлении, внешней напряженности полей(гравитационного, магнитного, электрческого)
Что будет, если смешать NaCl7 и ортоугольную кислоту?
Всё зависит от того, во что превратится кислота при 200-х тыс. атмосфер.
При давлениях, начиная с 20 гигапаскалей (ГПа), это 200 тысяч атмосфер, устойчивыми станут соединения Na3Cl, Na2Cl, Na3Cl2, NaCl3 и NaCl7 — такой вот букет соединений.
Сам, увы, даже близко не химик, поэтому даже банальные истины крайне приветствуются (ну, ХЗ, учебник химии за первый курс, например).
Симамура Углеродные волокна
Morgan Carbon fibers and their composites хорошая книга
Варшавский Углеродные волокна тут больше по получению и свойствах самих волокон.
Soo-Jin PArk Carbon fibers книга не понравилась, много банальщины и объяснений очевидных вещей, но тебе из-за этого может подойти.
Chung Carbon Fiber Composites небольшая, но насыщенная книга
Чтоб получить бром из бромида нужен любой оскислитель и кислая среда или обязательно нужна серная кислота?
Примерно то же, как если бросить усы единорога в молоко лягушки.
Собственно, потому, что ни при каких условиях они не будут термодинамически самой стабильной фазой.
Благодарю тебя от всей души, анон!
Но почему они тогда существуют? А не превращаются сразу же в графит, уголь, алмаз, карбин или какая там стабильная фаза?
>не превращаются сразу же
>>387156
>потому, что
>не будут
>термодинамически
>самой стабильной фазой
выкинул мяч с 10 этажа, а он на высоте 4 этажа завис в воздухе и никак не хочет дальше падать к земле(минимуму энергии)
Почему алмаз существует при нормальных условиях? Он при них существовать не должен, но он об этом не знает.

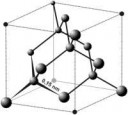

Каждый атом углерода в структуре алмаза расположен в центре тетраэдра, вершинами которого служат четыре ближайших атома. Именно прочная связь атомов углерода объясняет высокую твёрдость алмаза.
А теперь ты, ПОКАЖИ СВОИ АЛМАЗЫ.
Да хуй его знает почему, вроде все системы стремятся к минимуму энергии, но почему-то все атомные ядра не распадаются/синтезируются до Fe-56
Да мы вообще все стремимся к тепловой смерти, но алмаз-то только потому и не превращается в графит, что кинетически стабилен
тонкая полиэтиленовая плёнка - это энергетический барьер(ну тот про который говорят, когда поясняют за катализаторы, понять бы еще что это такое) или что-то другое?
Это - просто, аналогия.
Материал ПЭТ-тары (полиэтилентерефталат) растворяется при 40-150 °С в ацетоне, бензоле, феноле, толуоле, циклогексаноне, этилацетате, четыреххлористом углероде, хлороформе.
Что тебя смущает? Вопрос сформулирован по-мудовому потому что первокурсник
Смешно
проиграл и закрыл вот на этом месте
>Подтвержу слова анона выше про то, что сами химики до конца не понимают реакции, а иногда и с самого начала не понимают.
Я приведу вам очень простой пример, сейчас весь состав химиков пойдет резать вены от осознания своей ничтожности и некомпетентности.
Итак: почему NaCl растворяется в воде, но не растворяется в изопропаноле?
Соответствующие учебники а также статьи интересующих лабораторий. Кроме того, в лабах наверняка должны проводиться дни открытых дверей.
>>388248
Опять этот чудила, хваставшийся чтением википедии.
Любой учебник по физхимии к примеру Краснов или Эткинс. Если это осилил, то Кубасов хим кинетика и катализ и Эмануэль и Кнорре курс химической кинетики. По термодинамике Еремин (у него и по кинетике есть вроде) и Полторак.
Добавлю «Химию элементов» Гринвуда (годная неорганика/элементоорганика), «Органическую химию» Клайдена (крайне вменяемое пояснение за механизмы). С русскоязычным изданием обоих есть некоторые проблемы, но на торрентах оба есть.
Алсо, по физхимии (не упомянута) на начальном уровне нормально зайдет «Теоретическая и математическая химия» Еремина для продвинутой школоты; далее неплох будет Эткинс или тот же Еремин.
неразветвлённые алканы с CH4 до C4H10 являются газами, с C5H12 до C13H28 — жидкостями, а начиная с C14H30 и далее — твёрдыми веществами.
>Физические и химические свойства не сильно меняются, когда n становится большим.
В этом и суть полимеров. Попробую уточнить вопрос того анона: допустим, для цепей какой длины относительная разность температур плавления гомологов будет ниже одного процента?
>>384456
>этот полипептид нерастворим в воде, совсем, он образует КОЛЛОИДНЫЙ раствор и относится к ограниченно набухающим коллоидом
Какая истинная растворимость у твоего полипептида? Как выше заметили, он липофилен, но из-за того, что у этой большой молекулы одна половина выражено липофильна, а другая - выражено гидрофильна, происходит консолидация отдельных молекул в кучу.
Однако, эта молекула имеет истинную растворимость в воде. Бензол, например, нерастворим в воде аж на целых 1.8 г/л при 25°C.
Соли жирных кислот, в простонародии - хозяйственное мыло, в высоких концентрациях растворяются в воде с образованием мицел. Однако, они имеют ненулевую растворимость в воде, которая сильно повышается по мере повышения температуры.
Все, что ты сам знаешь про упомянутый - это что он нерастворим в воде и образует колоидные растворы. Помолился, свечку поставил, закрыл книжку, пошел спать. Но ты не знаешь, какая у него истинная растворимость - бля буду.
Все, я высказался, теперь можешь обратно в свой храм возвращаться.
>>384459
>Даже в учебнике глинки написано, что точно предсказать растворимость веществ в друг друге не возможно. Есть конечно теории, пресказыващие это, но со 100% вероятностью не скажешь
А не нужна 100% точность. Если предсказуемая растворимость будет в 2 раза отличаться от реальной, то это уже будет отличный результат. Такая точность вполне достижима для веществ без ебанутых кристалических решеток (вспоминаем знаменитое NaCl/NaBr/NaI+ацетон).
>>384473
>этот поехавший "разработал" свою теорию, однако его тут обоссали.
Ты мне напоминаешь бабу, которая гордится своим папиком, который пихает ей свой хуй в рот и кончает на лицо. Умываешь лицо, одеваешься, и выходишь с гордо поднятым лицом - ты в высшем обществе.
>>384452
>>Чем больше хвост, тем хуже притягивается
>Почему?
Молекулы ионных веществ предпочитают взаимодействовать по ионным связям, молекулы алканов имеют высокую поляризуемость и предпочитают взаимодействовать с диполями и высокополяризуемыми веществами. Насыщенная углеводородная цепь спирта почти не притягивается к соли, и при этом притягивается таким же углеводородам. Удельная сила притягивания спирта к соли, таким образом, снижается по мере удлинения углеводородной цепи.
>>384730
Серебряный тигель?
>>384456
>этот полипептид нерастворим в воде, совсем, он образует КОЛЛОИДНЫЙ раствор и относится к ограниченно набухающим коллоидом
Какая истинная растворимость у твоего полипептида? Как выше заметили, он липофилен, но из-за того, что у этой большой молекулы одна половина выражено липофильна, а другая - выражено гидрофильна, происходит консолидация отдельных молекул в кучу.
Однако, эта молекула имеет истинную растворимость в воде. Бензол, например, нерастворим в воде аж на целых 1.8 г/л при 25°C.
Соли жирных кислот, в простонародии - хозяйственное мыло, в высоких концентрациях растворяются в воде с образованием мицел. Однако, они имеют ненулевую растворимость в воде, которая сильно повышается по мере повышения температуры.
Все, что ты сам знаешь про упомянутый - это что он нерастворим в воде и образует колоидные растворы. Помолился, свечку поставил, закрыл книжку, пошел спать. Но ты не знаешь, какая у него истинная растворимость - бля буду.
Все, я высказался, теперь можешь обратно в свой храм возвращаться.
>>384459
>Даже в учебнике глинки написано, что точно предсказать растворимость веществ в друг друге не возможно. Есть конечно теории, пресказыващие это, но со 100% вероятностью не скажешь
А не нужна 100% точность. Если предсказуемая растворимость будет в 2 раза отличаться от реальной, то это уже будет отличный результат. Такая точность вполне достижима для веществ без ебанутых кристалических решеток (вспоминаем знаменитое NaCl/NaBr/NaI+ацетон).
>>384473
>этот поехавший "разработал" свою теорию, однако его тут обоссали.
Ты мне напоминаешь бабу, которая гордится своим папиком, который пихает ей свой хуй в рот и кончает на лицо. Умываешь лицо, одеваешься, и выходишь с гордо поднятым лицом - ты в высшем обществе.
>>384452
>>Чем больше хвост, тем хуже притягивается
>Почему?
Молекулы ионных веществ предпочитают взаимодействовать по ионным связям, молекулы алканов имеют высокую поляризуемость и предпочитают взаимодействовать с диполями и высокополяризуемыми веществами. Насыщенная углеводородная цепь спирта почти не притягивается к соли, и при этом притягивается таким же углеводородам. Удельная сила притягивания спирта к соли, таким образом, снижается по мере удлинения углеводородной цепи.
>>384730
Серебряный тигель?
>Уксусный ангидрид легко и просто синтезировать.
Рили? И как жи? Неужели из ацетонитрила? Или ты про старый дедовской метод через серу, который вонючий и хитровыебаный? (читай - никто уже не помнит, как он правильно делается)
>>386159
Муравьиная кислота очень легко осаждается щелочью. Подходящая для твоих нужд щелочь продается в любом хоз маге.
>>386185
>Все заебок, но спирт вероятно гидролизный непочищеный
Двойная перегонка на метровой елочной колонке даст солидный прирост в чистоте. Изопропанол там по прежнему останется, от него никуда не денешься.
Кстати, тут в треде годную тему подкинули про брагу. Чем с аптечными пузырями возиться - лучше наболтать в бочке турбодрожей с сахаром, с литра не меньше 140 мл получается.
>>386193
Стекло в совке было разное. Охуенно разное. У меня есть колекция такого говна из советского союза, которое вам в страшном сне не снилось. Одна из ключевых проблем советского стелка - вплоть до самого развала только один-два завода делали посуду из боросиликата. Я говорю про победу труда. Этот же завод наверное единственный, кто делал терпимые шлифы.
На остальной посуде шлифы косые-кривые, и самый большой батхерт со стенок в 0.2 мм толщиной, которые трескаются просто от того, что ты продемонстрировал недостаточно уважения к ним, когда ложил их на твердую поверхность.
Такие тонкие стенки сделаны не зря, потому что для изготовления посуды использовалось говно вместо стекла, и если сделать стенку толще - она лопнет от перепада тепературы. Но да, в итоге она лопается от перепада, потому что там тоньше, а в другом месте толще.
>техника бытовая вся заточеная под бытовой ремонт с конвеера
:) Советский союз последних примерно 15 лет - это кромешный пиздец. Самые громкие серийные убийцы пришлись именно на этот период: отравительница иванютина, нагиев, чикатило (особено красива история с ошибочно расстрелянным кравченко вместо чикатило). Крупнейшая в мире авария на ЧАЭС, самая ебанутая афганская война - все это было в последние 15 лет. Всем на все похуй, никто ни за что не несет ответственности. Как выдул тебе стекло - так и будешь пользоваться. А потому что выбора все равно нету, бг-г-г. Скажи спасибо, что на морозе на улице не трескается.
>>386231
>Не читай советское говно, лучше вообще никогда не трогай ничего советского, это лютый пиздец.
Западное говно трогать - тоже не особо лучший вариант, если че.
>>386389
>Качаешь рабочую программу с сайта министерства образования, сморишь книги и пиздуешь в библиотеку, либо на какой-нибудь трекер.
Ты забыл, что рабочая програма нужна только для того, чтобы отуплять и делать послушных рабов с конвеера, выполняющих работу по строго описаному алгоритму. Она никак не заточена на самостоятельное, и тем более на обучение.
>>386898
Нам в инстиутте с ходу дали програму на 150 строк кода - все учащиеся охуели, они никогда не кодили толком вообще. Это типа известный прием, суть заключается в том, что ты должен просто повторять все по шаблонам, главное - не пытаться ничего понять. Почему-то мне кажется, что там львиная доля вашей групы не поняла, что к чему в этих задачках.
>>387016
Солянка и бихромат дают хромил хлорид. Азотная кислота сама окисляет и выдает оксиды азота на выходе. Фосфорная? Может быть.
>>388248
>Итак: почему NaCl растворяется в воде, но не растворяется в изопропаноле?
Нехуй тут под меня косить. Цитируешь - оформляй как цитату.
>>388523
>Опять этот чудила, хваставшийся чтением википедии.
В википедии не объясняется, почему натрия хлорид нерастворим в изопропаноле. Об этом говорят только на дваче.
>>389105
У мета подтвержденая нейротоксичность на высоких дозах. Мозги сгорают к хуям.
>Уксусный ангидрид легко и просто синтезировать.
Рили? И как жи? Неужели из ацетонитрила? Или ты про старый дедовской метод через серу, который вонючий и хитровыебаный? (читай - никто уже не помнит, как он правильно делается)
>>386159
Муравьиная кислота очень легко осаждается щелочью. Подходящая для твоих нужд щелочь продается в любом хоз маге.
>>386185
>Все заебок, но спирт вероятно гидролизный непочищеный
Двойная перегонка на метровой елочной колонке даст солидный прирост в чистоте. Изопропанол там по прежнему останется, от него никуда не денешься.
Кстати, тут в треде годную тему подкинули про брагу. Чем с аптечными пузырями возиться - лучше наболтать в бочке турбодрожей с сахаром, с литра не меньше 140 мл получается.
>>386193
Стекло в совке было разное. Охуенно разное. У меня есть колекция такого говна из советского союза, которое вам в страшном сне не снилось. Одна из ключевых проблем советского стелка - вплоть до самого развала только один-два завода делали посуду из боросиликата. Я говорю про победу труда. Этот же завод наверное единственный, кто делал терпимые шлифы.
На остальной посуде шлифы косые-кривые, и самый большой батхерт со стенок в 0.2 мм толщиной, которые трескаются просто от того, что ты продемонстрировал недостаточно уважения к ним, когда ложил их на твердую поверхность.
Такие тонкие стенки сделаны не зря, потому что для изготовления посуды использовалось говно вместо стекла, и если сделать стенку толще - она лопнет от перепада тепературы. Но да, в итоге она лопается от перепада, потому что там тоньше, а в другом месте толще.
>техника бытовая вся заточеная под бытовой ремонт с конвеера
:) Советский союз последних примерно 15 лет - это кромешный пиздец. Самые громкие серийные убийцы пришлись именно на этот период: отравительница иванютина, нагиев, чикатило (особено красива история с ошибочно расстрелянным кравченко вместо чикатило). Крупнейшая в мире авария на ЧАЭС, самая ебанутая афганская война - все это было в последние 15 лет. Всем на все похуй, никто ни за что не несет ответственности. Как выдул тебе стекло - так и будешь пользоваться. А потому что выбора все равно нету, бг-г-г. Скажи спасибо, что на морозе на улице не трескается.
>>386231
>Не читай советское говно, лучше вообще никогда не трогай ничего советского, это лютый пиздец.
Западное говно трогать - тоже не особо лучший вариант, если че.
>>386389
>Качаешь рабочую программу с сайта министерства образования, сморишь книги и пиздуешь в библиотеку, либо на какой-нибудь трекер.
Ты забыл, что рабочая програма нужна только для того, чтобы отуплять и делать послушных рабов с конвеера, выполняющих работу по строго описаному алгоритму. Она никак не заточена на самостоятельное, и тем более на обучение.
>>386898
Нам в инстиутте с ходу дали програму на 150 строк кода - все учащиеся охуели, они никогда не кодили толком вообще. Это типа известный прием, суть заключается в том, что ты должен просто повторять все по шаблонам, главное - не пытаться ничего понять. Почему-то мне кажется, что там львиная доля вашей групы не поняла, что к чему в этих задачках.
>>387016
Солянка и бихромат дают хромил хлорид. Азотная кислота сама окисляет и выдает оксиды азота на выходе. Фосфорная? Может быть.
>>388248
>Итак: почему NaCl растворяется в воде, но не растворяется в изопропаноле?
Нехуй тут под меня косить. Цитируешь - оформляй как цитату.
>>388523
>Опять этот чудила, хваставшийся чтением википедии.
В википедии не объясняется, почему натрия хлорид нерастворим в изопропаноле. Об этом говорят только на дваче.
>>389105
У мета подтвержденая нейротоксичность на высоких дозах. Мозги сгорают к хуям.
>Ты мне напоминаешь бабу, которая гордится своим папиком, который пихает ей свой хуй в рот и кончает на лицо. Умываешь лицо, одеваешься, и выходишь с гордо поднятым лицом - ты в высшем обществе.
>Ятибяпириспорел!!!
Ожидаемо. Так как из Ван-дер-Ваальсовых взаимодействий следует меньшая растворимость хлорида натрия в воде по сравнению с изопропанолом?
>В википедии не объясняется, почему натрия хлорид нерастворим в изопропаноле. Об этом говорят только на дваче.
>
Что не мешало тебе с апломбом приводить ссылку на неё.
>оксид лития должен перейти в гидроксид с образованием кислорода
Не будет тебе кислорода.
Li2O + H2O = LiOH
>Получаю гидроксид лития растворенный в воде.
Да.
>Сушу и получаю оксид.
>Прокаливаю и получаю карбонат.
Вот оксид, как раз, из гидроксида,
ты получишь только при прокаливании в инертной атмосфере (H2).
Там идёт реакция, обратная той, что выше.
А карбонат лития получить можешь при нагревании оксида в углекислой атмосфере до 500 градусов Цельсия.
Но смотри не переборщи с тепмературой, потому что при 720 градусов Цельсия - карбонат
разлагается в оксид и углекислый газ.
А вообще, батарейку -> в газировку и высушить всё это дело, не?..
Зачем тебе карбонат?А так вроде все верно должно быть.
Порядочный работник должен с 8 до 17 трудиться, вечером бухать или сидеть перед телевизером, а по выходным ходить на футбол или на природу с семьей или друзьями. Нехуй тебе химией заниматься, понел, да? Это официальный посыл властей, наркоманы тут не при чем - они были всегда, но почему-то никто об это не жаловался.
>>389631
>Так как из Ван-дер-Ваальсовых взаимодействий следует меньшая растворимость хлорида натрия в воде по сравнению с изопропанолом?
Тебе стоит отвечать на то, что я уже написал про удельное притяжение. Или тебе объяснить, почему два вещества не растворяются друг в друге, если взаимодействие молекул одинаковых веществ намного сильнее, чем взаимодействие разных? У меня есть ощущение, что некоторые сидящие тут не читают даже википедии, мол "я в институте в 1980 году десять книжек прочитал - я теперь все знаю".
>>389632
>Что не мешало тебе с апломбом приводить ссылку на неё
На что предложишь ссылку приводить? На бумажную книгу и страницу в ней?
"В своём первоначальном значении слово «апломб», употреблённое в характеристике человека как личности, несло в себе сугубо положительную нагрузку. В конце XIX — начале XX века, согласно «Энциклопедическому словарю Брокгауза и Ефрона», апломбом называли «уверенность в действиях и находчивость в речи и в обращении с людьми»[1]. Такое же определение (слово в слово) дано и в Словаре иностранных слов, вошедших в состав русского языка под редакцией А. Н. Чудинова (1910 год). Так, например, говоря «британский апломб», подразумевали врождённое британское спокойствие и умение «держать удар».
Однако в XX веке употребление слова «апломб» применительно к персоне или организации приобрело негативную окраску. Филолог Н. Г. Комлев в своём «Словаре новых иностранных слов» описывает апломб следующими словами: «чрезмерная самоуверенность в поведении, в обращении с кем-либо»[2]. Апломб употребляется в одном ряду со словами «высокомерие», «заносчивость», «амбиция», «гонор» и т. п."
Сколько сидящих тут знает смысл слова "апломб"? Несмотря на появление седых волос в бороде, я до сих пор не знаю такого.
Порядочный работник должен с 8 до 17 трудиться, вечером бухать или сидеть перед телевизером, а по выходным ходить на футбол или на природу с семьей или друзьями. Нехуй тебе химией заниматься, понел, да? Это официальный посыл властей, наркоманы тут не при чем - они были всегда, но почему-то никто об это не жаловался.
>>389631
>Так как из Ван-дер-Ваальсовых взаимодействий следует меньшая растворимость хлорида натрия в воде по сравнению с изопропанолом?
Тебе стоит отвечать на то, что я уже написал про удельное притяжение. Или тебе объяснить, почему два вещества не растворяются друг в друге, если взаимодействие молекул одинаковых веществ намного сильнее, чем взаимодействие разных? У меня есть ощущение, что некоторые сидящие тут не читают даже википедии, мол "я в институте в 1980 году десять книжек прочитал - я теперь все знаю".
>>389632
>Что не мешало тебе с апломбом приводить ссылку на неё
На что предложишь ссылку приводить? На бумажную книгу и страницу в ней?
"В своём первоначальном значении слово «апломб», употреблённое в характеристике человека как личности, несло в себе сугубо положительную нагрузку. В конце XIX — начале XX века, согласно «Энциклопедическому словарю Брокгауза и Ефрона», апломбом называли «уверенность в действиях и находчивость в речи и в обращении с людьми»[1]. Такое же определение (слово в слово) дано и в Словаре иностранных слов, вошедших в состав русского языка под редакцией А. Н. Чудинова (1910 год). Так, например, говоря «британский апломб», подразумевали врождённое британское спокойствие и умение «держать удар».
Однако в XX веке употребление слова «апломб» применительно к персоне или организации приобрело негативную окраску. Филолог Н. Г. Комлев в своём «Словаре новых иностранных слов» описывает апломб следующими словами: «чрезмерная самоуверенность в поведении, в обращении с кем-либо»[2]. Апломб употребляется в одном ряду со словами «высокомерие», «заносчивость», «амбиция», «гонор» и т. п."
Сколько сидящих тут знает смысл слова "апломб"? Несмотря на появление седых волос в бороде, я до сих пор не знаю такого.
Я тебе еще раз повторяю, что они не долбоебы, а это точный расчет на подавление любительской химии с минимальным ущербом для промышленной химии. Например, никто никогда мне не сможет рационализировать запрет марганцовки или серной кислоты. Наркоманам и взрывотехникам эти запреты почти никаких препятствий не создали, зато создали огромный геморой даже честным лабам.
Серная кислота до недавнего времени была запрещена лишь в рашке. Марганцовкой эфедрин окисляют. Соляная запрещена только в рашке
Всем похуй на химиков любителей. Просто власти долбоебы. А у нас в стране еще и мзду за неправильное хранение прекурсоров требуют
В европе дохуя всего из за терористов позапрещали. При чем соляная кислота легальна. В австралии власти просто ебнутые. Стоит вспомнить историю с дигидроген монооксидом. Его хотели запретить чиновники из австралии. Техасцы отбитые на голову. У них даже закон на счет секс игрушек есть
Источника высокоорганизованного тероризма, то есть, единичные точные эфективные акции с большим резонансом, в мире ровно два: это западные спецслужбы и российские спецслужбы. Никакой таджик не отдаст свою квартиру под залог кредита, на который будет устроена акция.
Тогда мы приходим к вопросу: а каким образом запреты химикатов в европе мешают хорошо финансируемым терористам, получающим информацию от российской разведки? Это раз, запомнили вопрос.
Два: аутогенные терористы. Допустим, черножопые господа, которых любезно пригласили в европу (ну то есть всякие германии, которые зовут к себе чурок), решили какого-то хуя кого-то подорвать или убить. Скорее всего этим господам даже кто-то помог. Посмотрим, что предпринимают против них власти:
Regulated substances and concentration thresholds
hydrogen peroxide:12% w/w
nitromethane: 30% w/w
nitric acid: 3% w/w
sodium chlorate: 40% w/w
potassium chlorate: 40% w/w
sodium perchlorate: 40% w/w
potassium perchlorate: 40% w/w
Reportable substances
ammonium nitrate
acetone
hexamine
sulphuric acid
potassium nitrate
sodium nitrate
calcium nitrate
calcium ammonium nitrate
Здесь я соглашусь, что действительно, это меры, которые предназначены только против глупых чуркобесов, которые не способны ничего выдумать, кроме как в тупую идти "дайте мне три мешок аммоний нитрат и бензина - я выращивать помидоры". ну по крайней мере это тянет на попытку, окай.
>>389764
Вообще, наркоманов нужно убивать. Это не люди. Нормальные люди выпивают, ну курят сигареты, но наркотики - это все, конец, нет пути назад.
>>389765
Малаца, шаришь. Вспоминаем истории о том, как людей садили за подготовку к теракту после обнаружения при обыске полграма пороха или следов пероксида ацетона в ацетоне.
Охуеть и кальций нитрат запретили. Остался тока магний нитрат, из которого обменками можно другие получить. Алкоголь это тоже наркотик как бы. Ну да ладно я сваливаю с двощей на тематические форумы. Тут небезопасно
А как из растительного масла?
Двачую этого. И в целом тот же тексас это мурриканская мекка барыг из мексики, они оттуда все хуярят фурами, и мет и коку и все все все. Но в основном мет. От того там и запрущино все.
Но я вспомню историю про чувака который хотел собрать атомный реактор, и так собрал. Купил даже радиоактивные материалы нужны, его не остановило ничего. В итоге у него что-то пошло не так и его дом потом чистили от радиационного загрязнения за сотни тысяч далларов с вывозом грунта.
Ананас, я тебе простой пример приведу. Вот представь что живет с тобой, в одном многоквартирном доме молодой и шутливый пиротехник, и ебашит он перхлораты и кисы м мамкиной посуде, мешая стальной ложкой, промывая своим хуем и вообще пошла ты нахуй техника безопасности ебаная, чем кончится? И второй вариант, живет с тобой так же рядом не молодой и серьезный дядя, он крут и его погоняло хазинберг, а тот кто знает химию, тот знает что хазенберги чаще всего заканчивают свою жизнь в реанимации или ожоговом. Вот нахуй оно тебе надо? Я понимаю бугурт юриков, но это вынужденная мера чтобы долбоебы и наркоманы не взрывали вас и не травили, увы блять.
А муррика вообще веселая страна, у них в каждом штате свои приколы. Без шуток, заебись вообще.
Что не мешало мне рядом с домом уебать 10 г первичного инициирующего ВВ.
Ты можешь из того что осталось запилить, то что тебе нужно
>если взаимодействие молекул одинаковых веществ намного сильнее, чем взаимодействие разных
А как ты это предскажешь?
Например связь ртуть-ртуть куда выгоднее чем ртуть-целлюлоза, поэтому капля ртути на деревянном столе имеет шарообразную форму
Связи основаны на взаимодействии электронов разных конфигураций и ядер. Если у нас есть статический диполь, то можно ожидать его взаимодействия с другими диполями разных видов.
Силы дисперсионного притяжения (мгновенный диполь-наведенный диполь) с малым кол-вом других функциональных групп весьма хорошо предсказываются скалярными расчетами. Хуже всего онными предсказываются сильно зависящие от пространственной структуры ионные взаимодействия (финкельштейн, пептиды).
Например, мне не нужны никакие экспериментальные данные для того, чтобы сказать, что 3-этил-4-пропил-гексан-2-ол имеет низкую растворимость в воде, и даже с неплохой точностью посчитать эту растворимость.
Можете конкретнее и подробно объяснить процесс разложения?
При нагревании глицерина в присутствии какой-нибудь кислоты происходит двойная дегидрация, в результате чего две двойных связи по сути и представляют собой этот самый акролеин.
Что тут потерял формальдегид - в душе не ебу. Там точно нет аллилового спирта в списке?
Сам спросил - сам отвечаю: акролеин - это продукт алдольной конденсации формальдегида и ацетальдегида.
>>390351
т.е. жидкость в вейпах, нагреваясь, подвергается двойной дегидрации, и получившиеся две связи - ацетальдегид и формальдегид?
Химию учи, хуйню пишешь. Или найми себе химика-консультанта, который тебе будет все разжевывать.
я тут и спрашиваю поэтому как бы.
нахуй мне нанимать кого-то? просто возник единичный вопрос.
я же не заставляю тебе разжёвывать.
Есть даде реакция получения акролеина или аллилового спирта из глацерина. Пропиленгликоль тоже подвергается дегидратации однако в гораздо меньшей степени с образованием пропилового альдегида
Как диванный химик-теоретик пишу что надо кусок алюминия, железа/железной ржавчины, железо нагреть и растереть в порошок, алюминий тоже растереть в порошок, смешать и готово. Но я не уверен на счёт алюминия. Возможно он успеет слишком сильно окислиться.
Какой сульфонат? Что именно интересует?
Человек, который придумал делать эти жидкости на основе глицерина, явно был не очень знаком с органической химией. Пропиленгликоль ещё ладно, а вот с глицерином действительно промах.
Нужно нанести это черное тело на медную/алюминиевую фольгу, я собираюсь сделать солнечный коллектор.А для этого надо чтобы он испускал излучения меньше чем поглощал. А для этого надо самое черное тело которое только возможно. Так как создать на коленке вантаблек я не могу, прошу совета у местных менделеевых.
Я нашел как с помощью нитратов, кипятильника и насоса можно медь покрыть чОрным оксидом меди. Но это требует ебли с температурой и поливкой.
Срочный вопрос
Нужно вещество, которое при контакте с водой быстро(!) затвердевает
Завтра турнир, нужен самозалатывающийся водолазный костюм
Пришла в голову идея между двумя слоями костюма разместить искомое вещество, чтобы оно закупоривало дыру при проколе
Выручай, двач, весь инет перерыл, знание химии- 0
Герметик для камер.

Тебе зачем? Синтезировать можно много чего, но некоторые вещи только 1 раз.
- нахуй было банить МЭК?
- где его теперь можно найти, пусть даже разбавленный?
Сам хз. Ацетон еще объяснить можно. Это хз.
Сделать его можно пиролизом смеси ацетата кальция и пропионата кальция. Ацетат бери с избытком
Я тебе даже больше скажу - не только кальция. Но мне на данный момент похую препаративный синтез МЭК - меня интересуют простые источники, такие же, какие сейчас повсюду есть для ацетона, благодаря чему ацетоном можно чуть ли не посуду мыть (если жаба не душит мыть посуду растворителем по 400 рублей за литр).
Можно сделать серную кислоту, окисляя диоксид серы перекисью, можно сделать негашенную известь при помощи печки, но все это требует интенсивного предолинга, а я еще не настолько поехал.
>ацетон
Может ли он растворять органику(кожу, нервные, мышечные ткани, жировую ткань, кости(есть ли что -нибудь что может растворять кости, кроме плавиковой кислоты, фтора и соединений фтора вообще) и т.д.)? Не моментально конечно, а за месяц там например. Просто интересуюсь, у меня трупов нету.
Чтобы осваивать забугорные технологии синтеза, очевидно.
http://forum.secret-r.net/viewtopic.php?f=3&t=6183
Алсо
> Вот тут на форуме говорят, что не существует какого либо заговора против человечества – Наивные, Глупые и доверчивые – как дети. Я всё ждал, ждал – когда на этом форуме, или на другом, или вааще, дорогие мои, в вашем спящем царстве кем ни будь, будет поставлен ГЛАВНЫЙ вопрос, который должен стоять всё время (как я считаю) перед человеком мыслящим – но не дождался. И этот вопрос должен был быть кем либо поставлен именно перед собой как индивидуальностью - а не перед определённой группой – ибо любой стайный интерес типа « мы ФСЕ как один, должны взять жопу в горсть и пойти в леса на великую битву с треклятыми Москалями !!!» - либо любой другой стайный интерес – является средством зомбирования Ботвы и увода от Главного Вопроса, нигде не обсуждаемого – не буду я сейчас отслеживать ВСЮ цепочку, откуда этот «ветер» познания добра и зла с праведной битвой за справедливость дует. А вопрос то Главный и простой – «Для чего должен жить человек?».
>
> Так как вопрос «для чего я живу?» ни разу не приходил в вашу голову, а если и приходил – то сразу же отсекался вашим умом – это и есть ответ на теорию заговора. Итак – «для чего живёт человек?». Есть ли какой смысл в его существовании?. Ответов то я особо и не жду – потому что вопрос если и залетал в башку, то сразу «глушился» в сознании – но тут на форуме Фсе про Фсё Знают – может и найдутся у кого какие мысли в их отсутствии – на Главный Вопрос? А я пока попытаюсь в следующем посте ответить заблуждающемуся в иллюзиях Йоде, на проблему технократического пути развития цивилизации – которую мы начали на ветке «Апокалипсис» - тем более что она касается поднятого мной вопроса.>
Пушо у меня вот что:
(2.5 г) / (55,84 г/моль) = 0,04477 моль (количество железа)
(0,04477 моль) / 4 = 0,011192 моль (количество гемоглобина)
(0,011192 моль) • (68800 г/моль) = 770,0573 г (масса гемоглобина)
(770,0573) г / (150 г/дм^3) = 5,13 дм^3 (объем крови)
Пашаны, я вернулся с новым вопросом.
Мне нужно черное покрытие для абсорбера. Я стою перед выбором дорогая медь или дешевый люминь.
При этом, я нашел как почернить медь с помощью натрий о аша.
Можно как то химическим путем почернить люминь?
Там чтото непонятное. Там точно есть рецепт хлоргексидина?
Вот в википедии https://en.wikipedia.org/wiki/Chlorhexidine#Synthesis
есть чтото, но я думаю что все условия не написаны, и я незнаю что там за вещества.
Смотря какого дома и смотря сколько смеси.
>Во время пожаров с высокой плотностью теплового потока возможно оплавление некоторых составляющих бетона.
>Так, при температуре 1100-1150 С происходит оплавление керамзита, при 1300–1500 С – полевых шпатов, входящих в состав гранитного заполнителя, при 1700–1710 С – кремнезема; при 2000–2050 С – глинозема.
Казалось бы, температуры даже обычного железоалюминиевого термита - достаточно, но что бы реально что то расплавить (кроме собственного термитного шлака) - нужна не только температура но и теплота, т.е. термита нужно МНОГО ...
Термическое разрушение железобетона происходит из-за потери прочности несущими металическими элементами констуркции, бетону же почти что похуй на твой термит.
Да, похоже действительно там много способов синтеза. жаль что по английски написано, придётся переводить не только в гугл переводчике
Ну ебана, ты химию в школе прогуливал? Книжки читать не любишь и ютуб не можешь открыть? Почему я пишу очевидные вещи? Зачем ты зашел итт?
Ну я подумал что карбон реагирует с ферум оксидом, выдиляется железо, но ведь железо не реагирует с калий нитратом
Карбоний окисляется, а нитрат окислитель.
Есть ли смысл поступать на гинеколога, если любишь ебаться и вообще голых тяночек?
ну поебаться то придется, это во всей медицине хватает

Я тебе отвечу так, вот например у крокодила в желудке не кислая среда, а щелочная, и он жрет все, переваривая кости.
Если водой промыть нацать раз то лучше будет?
google.com/patents
а я сделаю манипуляторы и буду из далека через провод, за бетонной стеной управлять реакцией.
>все реакции нитрования органики это пиздец
Не совсем так. Дофига вполне себе мягких и приятных нитрований, особенно когда продукт вполне себе стабилен. Ты, видимо, подразумевал синтез нитроэфиров. Вот это да, пиздец практически во всех случаях, может кроме нитрования целлюлозы, или какого-то подобного говна.
Если повезет то голову, и будет одним долбоебом меньше.
Химики, если в атмосферу попадет большое количество хлора (500 литров) накослько быстро он перейдет в форму безвредную для человеков и пингвинов?
ПДК хлора в атмосферном воздухе среднесуточная для людей — 0,03 мг/м³, плотность его при н. у. - 3,21 г/л, будет 1605 г, то есть надо подождать когда он растворится в 53500 м3 воздуха, это почти 38 на 38 на 38 метров куб. как быстро он будет растворятся - я незнаю. Это зависит от ветра, температуры (в Антарктиде, где большинство пингвинов, температура низкая, так что плотность хлора будет больше и хуже хлор будет диффундировать). К тому же безопасность зависит то высоты, чем выше его сбросить тем больше он будет растворятся и тем больше безопасность.
Я планирую одну хим реакцию провести с которой выход хлора будет аж 500 литров. Реакция будет идти в гараже и около него загороднего дома примерно пятнадцать минут.
Хочу последствия узнать.

>>393038
Если хлор - побочный продукт реакции, тебе стоит его утилизировать.
Можешь, переменный ток выпрямить, и через электролизёр раствор какой-нибудь щёлочи пропустить, получив водород.
А затем, спалить его в хлоре - получив растворимый в воде хлороводород.
http://files.school-collection.edu.ru/dlrstore/08d3a964-383d-9411-dba5-7fd6dc3bb676/index.htm
и, как следствие - соляную кислоту.
Алсо, можешь утилизировать хлор в ацетоном - получив хлороформ.
Потому, что хлор - ядовит.
Хлор — токсичный удушливый газ, при попадании в лёгкие вызывает ожог лёгочной ткани, удушье. Раздражающее действие на дыхательные пути оказывает при концентрации в воздухе около 6 мг/м³ (то есть в два раза выше порога восприятия запаха хлора).
ПДК хлора в атмосферном воздухе следующие:
среднесуточная — 0,03 мг/м³; максимально разовая — 0,1 мг/м³; в рабочих помещениях промышленного предприятия — 1 мг/м³.
Плотность воздуха: 1.225 грамм/литр
Плотность хлороводорода 1.477 грамм/литр (25 °C)
Плотность хлора - при нормальных. условиях. 3,21 грамм/литр;
Плотность водорода: 0,08987 грамм/литр, при нормальных условиях.
Растворимость хлороводорода, в воде - 72,4
Растворимость хлора - (20 °C) 0,96
Как видишь, водород, легче воздуха, а хлор и хлороводород - тяжелее.
Поэтому водород можешь поджигать разрядом при подаче снизу.
А растворять всё это - распылением воды сверху, к стенкам ёмкости, где горит водород в хлоре и отводом кислоты - снизу.
Если хлор - целевой продукт реакции, сожми его в баллоны.

>>393038
Если хлор - побочный продукт реакции, тебе стоит его утилизировать.
Можешь, переменный ток выпрямить, и через электролизёр раствор какой-нибудь щёлочи пропустить, получив водород.
А затем, спалить его в хлоре - получив растворимый в воде хлороводород.
http://files.school-collection.edu.ru/dlrstore/08d3a964-383d-9411-dba5-7fd6dc3bb676/index.htm
и, как следствие - соляную кислоту.
Алсо, можешь утилизировать хлор в ацетоном - получив хлороформ.
Потому, что хлор - ядовит.
Хлор — токсичный удушливый газ, при попадании в лёгкие вызывает ожог лёгочной ткани, удушье. Раздражающее действие на дыхательные пути оказывает при концентрации в воздухе около 6 мг/м³ (то есть в два раза выше порога восприятия запаха хлора).
ПДК хлора в атмосферном воздухе следующие:
среднесуточная — 0,03 мг/м³; максимально разовая — 0,1 мг/м³; в рабочих помещениях промышленного предприятия — 1 мг/м³.
Плотность воздуха: 1.225 грамм/литр
Плотность хлороводорода 1.477 грамм/литр (25 °C)
Плотность хлора - при нормальных. условиях. 3,21 грамм/литр;
Плотность водорода: 0,08987 грамм/литр, при нормальных условиях.
Растворимость хлороводорода, в воде - 72,4
Растворимость хлора - (20 °C) 0,96
Как видишь, водород, легче воздуха, а хлор и хлороводород - тяжелее.
Поэтому водород можешь поджигать разрядом при подаче снизу.
А растворять всё это - распылением воды сверху, к стенкам ёмкости, где горит водород в хлоре и отводом кислоты - снизу.
Если хлор - целевой продукт реакции, сожми его в баллоны.
Только там, если будешь утилизировать в HCl надо посчитать молярную массу для двухатомного хлора
из его атомной массы в таблице Менделеева,
и сопоставить её с массой двухатомного водорода
полученной из атомной массы водорода в таблице Менделеева -
для полной утилизации хлора.
А кислород - в воздух.
Если же выкинешь хлор в воздух, он пойдёт в низины, т. к. его плотность больше плотности воздуха.
К тому же, он малорастворим, и ты увидишь ядовитое одеяло зеленоватого цвета, даже на воде.
Охуительная история, а теперь отложи в сторону свои книжки и интернет, и попробуй сделать что-то своими руками.
А если сделать из двух диодов штуку, которая превращает переменный ток в пульсирующий то его можно использовать для электролиза?
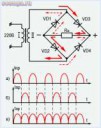
Если рукожоп, то лучше сделать это что-то хуями.
>>393047
Лучше из четырёх, а то из двух две полуволны потеряются.
И диоды - юзай побольше, а то от силы тока проходящей через них - зависит скорость получения водорода для электролиза.
Соли в электролите не растворяй, лучше щёлочь.
И переменный ток не юзай, а то будет смесь из водорода и кислорода - взрывоопасная.
Гремучий газ.
https://www.youtube.com/watch?v=nJK85-lPoO4
Поджигать водород в хлоре можешь с помощью свечи зажигания.
Да, и вот ещё... Смесь хлора и водорода реагирует со взрывом на свету, поэтому если будешь поджигать - делай это сразу, с постоянной подачей водорода в процессе его горения в хлоре. Не давай ему уйти вверх из-за высокой плотности и осесть там.
Вместо того, чтобы запускать ядерные ракеты, их подорвут в шахтах и на пусковых установках. Наполеон же взял Москву? Взял, а ночью кто-то ее поджог, чтобы не доставалась врагу. Вот тут также будет. Полыхнет Москва, задымится Воронеж, оплавится Краснодар...
FeCl3 + Al = AlCl3 + Fe
Хлор не выделется же.
Сам хлорид можешь получить и без газообразного хлора:
Fe(OH)3+3HCL=FeCL3+3H2O
FeO + HCl = FeCl2 + H2O
FeO(OH) + 3HCl = FeCl3 + 2H2O
Fe3O4 + HCl = FeCl2 + FeCl3 + H2O
Fe2O3 + HCl = FeCl3 + H2O
4FeCl2 + SO2 + 4HCl = 4FeCl3 + S + 2H2O
S + H2SO4 = SO2 + H2O
Ржавчина состоит из гидратированного оксида железа(III) Fe2O3·nH2O и метагидроксида железа (FeO(OH), Fe(OH)3).
Ну, и Fe + 2HCl -> FeCl2
Оставляют ли химические ожоги ДНК и РНК, если взять их голыми руками? Они же кислоты вроде.
>Можешь, переменный ток выпрямить, и через электролизёр раствор какой-нибудь щёлочи пропустить, получив водород. А затем, спалить его в хлоре - получив растворимый в воде хлороводород.
Зачем ты такой злой? Почему ты хочешь выпилить этого няшу? Данная реакция идёт со взрывом.
У меня вся рука ожогах тащемта.
Есть хим. состав цветного дыма (красный огонь)
KCIO3 - 42%
Sr(NO3)2 - 42%
ПВХ - 16%
Мне необходимо рассчитать коэффициент Демидова для каждого из элементов.
Как это делается? Дайте пожалуйста наводку. Что тут окислитель, а что горючее?
Соли хлорноватой кислоты (хлораты) — сильные окислители, в смеси с восстановителями взрывоопасны.
Значит хлорат калия - окислитель.
Нитрат стронция - восстановитель.
Если проценты по молям, то коэффициент Демидова - 1 к 1.
https://www.youtube.com/watch?v=vlpK-i-7-Bk#t=1m00s
>Влажная лакмусовая бумага показывает кислую реакцию
>лакмусовая бумага
Изыди. Именем отца и сына, и святого духа. Аминь.
>лакмусовая бумага
Чем тебе не нравится лакмусовая бумага?
Можешь использовать фенолфталеин.
>Изыди.
Куда? И почему Shift не нажал, а маленькой буквы Троицу назвать решил?
>У меня до сих пор тлеет огонек с того, что в большинстве книг и методичек до сих пор не освоили ни одного современного индикатора ph, где под современным я понимаю разработанный в последние 80 лет. Вот здесь http://window.edu.ru/catalog/pdf2txt/310/64310/35121?p_page=2 , например, уже знают про триарилметановые индикаторы начала прошлого века, которые перемежаются с бесполезными допотопными тропеолинами и фенолфталеином.
Современная лакмусовая бумага - это на самом деле бумага, пропитанная лакмоидом http://www.sigmaaldrich.com/catalog/product/aldrich/274720?lang=en с переходом окраски в интервале 4.4-6.4, что, как вы понимаете, весьма далеко от нейтрального 7.0, и даже несмотря на это она более полезна, чем настоящая лакмусовая.
>>378674
>например, уже знают про триарилметановые индикаторы начала прошлого века, которые перемежаются с бесполезными допотопными тропеолинами и фенолфталеином.
Пиздец дауны, такое разнообразие индикаторов необходимо чтобы подобрать для конкретных условий титрования индикатор, ошибка которого будет наименьшей. И это юзается в старых древних методиках, когда у тебя нихуя нет в лабе вообще. Сейчас рулят мультисенсорные системы по типу "электронный язык", управляемые нейросетями.
Я не промахнулся. То был мой пост. Фенолфталеин здесь мимо касы. Не считая уже того, что фенолфталеин, в общем-то, неудобен в незабуференом растворе, потому что небольшого кол-ва щелочи в таком случае достаточно, чтобы сделать сильнощелочной раствор фенолфталеина бесцветным. Его используют разве что потому что очень дешевый и везде есть.
>>393201
Очень удобно быть в курсе передовых систем, когда ты за них не платишь. Если бы я экстази мешками варил, то может быть я бы и подумал про электроный язык. Большинству же анонов никто не даст финансирования, потому приходится пользоваться химическими индикаторами.
Конечно же у тебя есть хроматограф с мас-спектрометром на выходе, но тут сидят аноны, которые побираются с хроматографией на бумаге, и для карбоксильных кислот какой-нибудь бромкрезоловый зеленый находится вне конкуренции.
Ну так что, кто ответит?
В водном растворе хлорида железа алюминий вымочить чтобы он стал темно серым, какой налет на олюминии будет?
Не нашёл слова окислитель в разделе про нитрат стронция на википедии
@
>Значит
>Нитрат стронция - восстановитель.
@
>Больше не давай советов
@
>Теперь, там нитрат стронция - служит окислителем

>>393409
Но ведь этот
>>393373
прав.
В пиротехнических смесях - нитраты действительно источники кислорода, а именно это важно для
>коэффициент Демидова
А использовать соли стронция - для окрашивания пламени - совершенно нормально!
Ну и самое главное, вопрос
>>393093
какой то странный.
Насколько я помню - коэффициенты Демидова - это табличные значения для упрошенных вычислений, когда качественный состав смеси мы предполагаем известным, а хотим рассчитать проценты:
>Подбор коэффициентов при расчете смесей (особенно с органическими горючими) требует много времени. В связи с этим А. Н. Демидовым было предложено пользоваться упрощающими вычисления подсобными таблицами, в которых указано, сколько граммов окислителя потребуется для выделения 1 г кислорода и какое количество горючего может быть окислено 1 граммом кислорода.
У тебя же, уже все известно. Можно конечно решить обратную задачу, но зачем?
А почитать, хотя бы
Шидловский А.А. "Основы пиротехники"
http://pirochem.net/index.php?id1=3&category=chemvvisost&author=shidlovskiy-aa&book=1954&page=21
ну или, как подсказывает КО, "Введение в пиротехнику" А.Н. Демидова
>Можно конечно решить обратную задачу, но зачем?
Кстати, для ее решения нужно быть уверенным, что кислородный баланс нулевой,ну или знать с каким избытком/недостатком взят окислитель/горючие.
Стронтат натрия тогда.
Эта хуита гореть не будет. И это уж точно не состав цветного дыма, отдаленно напоминает состав красного огня, но как уже сказали не хватает высокоэнергетичной горючки типа алюминий-магния, но их смеси с нитратом стронция из-за его гигроскопичности не рекомендуются и с хлоратами тоже.
современные штатные составы красного огня в гражданской пиротехнике как правило содержат
перхлорат калия
карбонат стронция
идитол
порошок алюмниево-магниевый
хлорорганика(ПВХ, ПХВ, твердые хлоропарафины, парлон)
рекомендую этот сайт
https://pirotehnika-ruhelp.com/
Да ему ж надо было коэффициент Демидова посчитать, а не эти ваши цветные дымы.
мне надо yбить не тех кто на стулья садится, а тех кто к поручням прикасается.
Спасибо, завтра синтезирую.
Технический углерод. Где его можно купить?
Тогда химия не для тебя.

Может тут быть?
Можно, но заебёшься потом от растворителя избавляться, ДХЭ гораздо менее летучий, чем ДХМ.
А что можно из легкодоступного взять вместо дмх?
Если например сначала сделать очень крепкий кофе, а потом подкислить это дело, добавить галоши и взболтать? По идее растворимость в кислой среде должна упасть и кофеин должен норм растворится в бензине. В интернете написано что кофеин хорошо растворим в органических растворителях, но не особо написано в каких.
Либо проще экстрагировать горячей водой, отстоять, отфильровать хорошо и перекристализовать просто охладив тк растворимость падает в 30 раз. В общем буду эксперементировать. Можно конечно пойти и купить рр для иньекций в ампулах, но это не наш метод.
Пиздец даун, вы хотя бы в школе учились? Если подкислить кофеин возрастёт резко его растворимость в воде. Добавь гидроксида натрия в крепкий кофе и тебе выпадет осадок основания кофеина (и других алкалоидов).

Щавелевую кислоту/оксалат калия - ты в специализированном хим.магазине покупал или как средство "бытовой химии" брал?
Купил в ленреактиве. Но техническая тоже пойдёт, я бы купил её, если бы продавалась.
Пищут что щелочь наоборот повышает растворимость. Ты по ходу сам не особо учился в школе.
>Растворимость в воде увеличивается при добавлении бензоатов, циннаматов, цитратов или салицилатов щелочных металлов. Бензоат например натриевая соль бензойной кислоты.
Тут дело явно не в pH, если только определённые соли улучшают растворимость.
>>394043
Лол, как ты думаешь, откуда происходит название алкалоид?
Маняврирование пошло.

>>394041
>... калоша точно не подойдёт. Она гораздо лучше растворит всякие смолы
Ой блядь! 21 век, интернет. До сих пор не знать (а если не знаешь не посмотреть в несколько кликов) как выделяют алкалоиды используя разную растворимость их солей/оснований в полярных/неполярных растворителях.
Я уже не говорю про то, что для любого природного алкалоида (кроме совершенной экзотики) в профильной литературе есть пропись выделения.
(На счет релевантности картинки - не уверен, 20 лет прошло.)
Дайте-ка инструкцию для даунов.
Честно гуглил, пропорций не нашёл
>как выделяют алкалоиды используя разную растворимость их солей/оснований в полярных/неполярных растворителях.
Ну и блять там нам написано возьмите ДХМ йобта, где я тебе его высру? Пиздец умные пошли.

>Пиздец умные пошли.
http://forum.xumuk.ru/index.php?showtopic=185951
- это по поводу чем заменить.
(я так и не понял чем тебе ДХЭ то не угодил?)
Но суть в том, что судя по этой фразе
>Если например сначала сделать очень крепкий кофе, а потом подкислить это дело, добавить галоши и взболтать? По идее растворимость в кислой среде должна упасть и кофеин должен норм растворится в бензине.
(если ты ее писал) ты нихуя, от слова "совсем" не пронял про
>разную растворимость их солей/оснований в полярных/неполярных
На что тебе и указал анон
>>394024
(не я).
Еще попробуй поискать альтернативные прописи (на английском общинная литература, в т.ч. и для "МамкиныхХайзенбергов").
Ну очевидный же дихлорметан. Ты не ходи в этот яндекс, там наркоманы, они тебя плохому научат.
>не пронял про
Да, я нихуя не понял, именно поэтому я пришел сюда, за мудрыми советами. Потому что в той литературе что я читал не было конкретных сведений, а где еще искать я не знаю, поэтому у меня 2 стула, на одном анон дроченный, на дром эксперимент с растворителем точеным. И да, я ему указал что растворимость алколоидов в воде по моей инфе растет в щелочной среде, пруфов по поводу неправильности моего мнения он доставить не смог. И я их не вижу итт до сих пор.
>Еще попробуй поискать альтернативные прописи
Вся надежда на заграницу, как обычно.
SCIентач исправляется, тебя уже обоссали и без меня.
>>394056
Ему больше Халецкий подойдёт, дикая древность, но примерно такими возможностями этот анон располагает.
Так вон же он, чёрный, видишь?
растворимость алколоидов в воде по моей инфе растет в щелочной среде, пруфов по поводу неправильности моего мнения он доставить не смог.
Пруфы тебе подвёз.
Кофеин, кофеин безводный. Легко растворим в горячей воде и хлороформе, умеренно (медленно) растворим в воде, мало растворим в этаноле 96%.
ФС 42-0248-07 ФС 42-0249-07
Кофеин бензоат натрия Описание. Белый порошок без запаха, слабо горького вкуса. Растворимость. Легко растворим в воде, трудно растворим в спирте.
Пруфы 173 статья ГФ XI
То есть в виде соли растворимость в воде кофеина в разы выше, чем в виде основания.
Единственный кто обоссался это ты, мань.
>>394105
И где тут пруфы, при том что я тебе писал дауну >>394042 вот этот пост.
>>394106
Давай конкретнее цитируй.
А пока будем считать ты обосрался раскукукаревшись ЧИМУ ВАС УЧАТ КОКОКО и неся хуйню про какие-то учебник по фарме, какие-то невнятные ссылки и обрывки с вики которые я итак читал.
Пиздец ты тупой.
>Ну очевидный же дихлорметан. Ты не ходи в этот яндекс, там наркоманы, они тебя плохому научат.
- Эту фразу расшифруй пожалуйста. А то непонятно:
Вот
>>393914
спрашивает - "Чем заменить дихлорметан (ДХМ)?"
Яндекс в первой(!) же ссылке - дает таблицу полярности и обсуждение - "Чем его заменить", что не так?
И тебе уже несколько раз сказали, что в общем случаи - растворимость солей алкалоидов в полярных (воде) больше, а в неполярных - меньше (для оснований - наоборот).
Конкретно это
>То есть в виде соли растворимость в воде кофеина в разы выше, чем в виде основания.
- тоже (на сколько я помню) верно, вот же дали пруф
>>394105
Как меня бесят эти тупые школьники. Почему Алкалоид назвали Алкалоидом? Что такое алкали-? Алкалоид почти всегда проявляет основные свойства! В 99% случаев простые соли алкалоидов легче растворяются в воде, чем основания алколоидов, поэтому, все где возможно химической структурой, препараты алкалоидов это не основания, а гидрохлориды!!!
Теперь по поводу моих пруфов. Там есть ссылки на две фармакопейные статьи, первая на кофеин основание где указана растворимость: УМЕРЕННО растворим в воде, вторая на кофеин-бензоат натрия, который ЛЕГКО растворим в воде. Тоже самое ты можешь найти для папаверина, морфина, атропина и прочих. Если для тебя Государственная фармакопея не пруф, тогда я уже не знаю.
Я не вижу пруфов того что кислая среда помогает лучшему растворению, дебила кусок. То что ты написал я и так знаю.
Бля буду, кислота способствует растворению щелочи в воде. На гидроксиде натрия попробовал только что.
Хорошая, годная статья. ХЗ, сколько труда у них ушло на эти исследования, не чета нынешнему говноварству в стиле "наша химия спасёт мир". Прикол в том, что классический E2 из учебника - сферический конь в вакууме. По факту, как тебе объясняют в этой статье, там целый континуум механизмов, от тех, в которых вначале отваливается уходящая группа, до тех, в которых вначале депротонируется бета-углерод. Четвертичные соли аммония способствуют отделению уходящей группы за счёт поляризации связи C-X, т.е. получается эдакий недоделанный E1, который в этой статье называют E2C. В ацетате тетрабутиламмония, помимо этого, ацетат-ион выступает в роли неплохого такого основания, ибо среда безводная, и анион сольватирован по минимуму.
Эээ братышка, какие пруфы? Вах мамой клянус! Вэк баранов не видать!
Самый сильный реагент для E2C - тетрабутиламмония бромид, который из всего списка - самый неосновной. Как я догадываюсь. авторы в статье как раз и подчеркнули, что эта соль путем совершенно иного, нежели свойственного алкоголятам E2H, довольно эффективно способствует произведению элиминирования. Для меня странно, что такая достаточно крупная по размерам шняга, как тетрабутиламмоний, способна соударяться в двумя реагирующими атомами (или кто там соударяется?).
Голый бромид-анион в апротонном биполярном растворителе таки является неплохим основанием. Механизм E2C кагбэ намекает, что от бимолекулярности там одно название, и цимес всё-таки в поляризации связи C-Br за счёт повышения ионной связи раствора. До чистого E1 всё-таки не дотягивает, однако. Учись воспринимать органику как набор кулинарных рецептов. Попытки "понять" зачастую приводят к появлению манятеорий исключительной сложности, и нулевой предсказательной силы.
Ацетон является более сильным основанием, чем ТБАБ. Механизм E2C не основывается на кислотно-основной реакции чего-либо, поскольку повышение кислотности любого из участвующих в элиминировании углеродов почти не влияет на скорость E2C.
Вопрос механизма этой реакции также важен для понимания, например, полупинаколиновой перегруппировки, где подобным образом уходит галогенид в кислой среде, очевидно также по причине атаки анионом по углероду с большим кол-вом заместителей на нем самом и на соседнем углероде.
Я не спорю с тем, что органика слабопредсказуема, но это обусловлено цифрами, количественной разницей в реакционоспособности различных соединений, которая приводит к тому, что одно соединение реагирует легко по нужному пути, а другое - очень тяжело, и преобладает побочная реакция. Или один реагент оказывается газообразным и крайне неудобным в лабораторном препаративном синтезе, а в промышленности наоборот, самые неудобные - твердые реагенты. Это и есть та самая обусловленность кухней, но качественные явления ты все равно можешь понимать, чтобы хотя бы ориентировать во всей кухне.
Какая-нибудь химия может вызвать каталепсию при вдыхании?

На пике интереса военных/спецслужб к нелетальным ОВ - были, кажется, синтезированы ингаляционные нейролептики (твердое вещество в аэрозоле), а если нейролептик имеет анти-дофаминергический механизм, то большая доза - должна, по идеи, вызывать медикаментозную каталепсию (как галоперидола нажраться).
А есть вообще книжки по нелетальным ОВ новеее "Химическое оружие на рубеже двух столетий"?
>книжки по нелетальным ОВ новеее "Химическое оружие на рубеже двух столетий"?
Новее монографии Николай Серафимовича? Не, не видел. Другое дело, что как раз кое какой экзотики, типа этого
>>394227
(по причине малоэффективности) - у него как раз и нет, кажется (точно не помню, давно читал).
Ну и понятно, постоянно новые ве-а синтезируют (или доходят руки изучить свойства уже синтезированных)
Фигово, может есть сайт какой по новым открытиям в этой области? Или тег по которому можно нагуглить научные статьи по теме
>может есть сайт какой по новым открытиям в этой области?
Врядли (раньше были любительские сайты, но все поимели проблемы)
Это (постоянное появление новых веществ) - фундаментальная организационная проблема. Например, относительно недавно (1998) синтезированный
https://ru.wikipedia.org/wiki/Bromo-DragonFLY
- лишь в ~5 раз слабее ЛСД.
Напомню, ЛСД - в разгар холодной войны - реально рассматривали как психохимическое оружие.
>Или тег по которому можно нагуглить научные статьи по теме
Сами вещества
https://pubchem.ncbi.nlm.nih.gov/
Статьи
https://www.ncbi.nlm.nih.gov/
Кто профессионально занимается, может подскажет лучший вариант.
>Ацетон является более сильным основанием, чем ТБАБ
Это очень хороший вопрос. В воде - однозначно, там pKa HBr = -9, а протонированного ацетона - где-то около -7. А вот в биполярных апротонных растворителях скорее всего наоборот. Точные цифры найти не получилось, но в ДМСО pKa HBr 0.9, т.е. почти на 10 единиц выше. Для протонированной органики pKa в ДМСО хоть и отличается от такового в воде, но всё-таки не настолько сильно.
>Механизм E2C не основывается на кислотно-основной реакции чего-либо
Таки взаимодействие C-H с основанием в переходном состоянии имеет место быть, иначе реакция не была бы бимолекулярной. Другое дело, что ослабление связи C-X за счёт повышения ионной силы раствора, похоже, играет куда большую роль.
Данные в статье говорят, что повышение основности аниона приводит к смене баланса механизмов, то есть, к переходу от E2C к E2H с изменением соотношения продуктов. Речь идет как об изомерах, так и о позже проведенных исследованиях кинетики на дейтрированных соединениях.
Ионная сила раствора - это сферический конь в вакууме. Свойства катиона говорят о том, что в реакции он не участвует и ни с чем не сталкивается, но дает фоновый положительный заряд для уравновешивания аниона. Способен ли жесткий щелочной катион?, который очень слабо взаимодействует с галидом, разорвать ковалентную связь галогенида с углеродом?
>Ионная сила раствора - это сферический конь в вакууме
Нннет. Чем выше ионная сила раствора, тем больше этот раствор способен стабилизировать ионы и сильно поляризованные структуры. Чем больше вокруг плавает других ионов, тем больше поляризована твоя молекула (ну или переходное состояние) за счёт взаимодействий типа ион-диполь, или ион-индуцированный диполь. Переход от E2C к E2H лишь означает, что переходные состояния поляризованы по-разному относительно слабополяризованного Е2. Сильно основные анионы в большей мере ослабляют связь C-H, чем C-X. При отсутствии сильных оснований в реакционной смеси, картина сдвигается в сторону ослабления связи C-X. Собственно, переход от E2 к E1 по мере увеличения ионной силы раствора - хорошо известный факт. В данной статье полного перехода к E1 не наблюдается, но есть сдвиг в этом направлении.
Я совсем нуб и не разбираюсь в стекле.
https://ru.aliexpress.com/item/500ml-24-29-Glass-Distillation-Apparatus-Laboratory-Chemistry-Glassware-Kit/32730867916.html
Воду, растворители, азотную кислоту.
Немного смущает красная пластиковая крышечка, там где вставляется термометр. Но если она не устойчивая - что-нибудь докуплю еще туда.
Набор норм но лично меня смутили.
1.Градусник. Збс, но зачем когда есть ик термометр?
2.Пластиковая крышечка как уже заметили итт. У тебя вероятнее всего её разьест к хуям.
3.Круглодонные колбы жи есть, хз как на это посмотрит таможня. Раньше их физикам покупать было низя, по крайней мере без паспорта как марганцовку.
1 - ну блеа, традиция.
2 - это да.
3 - Круглодонные колбы, специализировали под химические действия, как по мне лучше самые обычные плоскодонные.
Плоскодонные потом куплю, вместе с мешалкой. Пока я слишком ньюфаг для реакций где это может понадобиться.
>Круглодонные колбы жи есть, хз как на это посмотрит таможня. Раньше их физикам покупать было низя, по крайней мере без паспорта как марганцовку.
Расскажи прохладную. Я чет впервые такую хуйню узнал - чем провинились круглодонные колбы? Их же даже самому можно делать, лол.
Да, не разглядел. Пластиковая крышечка - это хуёво, кислоту она почти наверняка не переживёт, да и от хлорированных или ароматических растворителей скорее всего разбухнет и деформируется.
с стекловым дистелятором нужно быть аккуратным. его нужно крепить на стойку. стойки по 100 долларов. и без нее, если соорудить на соплях, упадет и разобьется, как у меня было.
стекло делают в россии.
Я раздобыл несколько совковых штативов.
Ты еще спроси почему используется 2 классификации одновременно.
Хной собрался красить?
Вот здесь (красят анилиновыми, после анодированния в серно-щавелевом электролите) поспрашивай
http://www.chipmaker.ru/topic/175647/page__st__40
Что происходит с молекулами высокой молекулярной массой(Белки, ДНК, РНК и т.д.) при огромных давлениях(20 ГПа или сколько там могут ячейки с алмазными наковальнями)? Распадаются на простые вещества, полимеризуются или что-то другое?
Что там у Декстер в шприце было? Из чего получают?
Мгновенно расползается, стоит только чуть надорвать? Целлофан.
>они не долбоебы
>расчет на подавление любительской химии с минимальным ущербом для промышленной химии
>Наркоманам и взрывотехникам эти запреты почти никаких препятствий не создали
>создали огромный геморой даже честным лабам
Взаимоисключающие параграфы во все поля.
Хуйня, я пробовал. Не горит такая смесь, возможно её надо как-то прессовать и предохранять алюминий от окисления.
Странный градусник, похоже спиртовой, в высокие температуры не умеет. Ебанутые пластиковые зажимы сломаются после пары использований, инфа 100%. К тому же, имхо, этот набор слишком дорогой. В китае вообще лабораторная посуда дорогая, у нас она стоит в полтора-два раза дешевле.
>как по мне лучше самые обычные плоскодонные
Не годятся для перегонки под вакуумом. Был случай, решил промыть стеклянный фильтр ацетоном, он подзабился смолой и плохо пропускал. Под рукой была плоскодонка на 250, ну я подумал "да ладно, че ей будет, я только на полсекунды присосусь водоструем, выдержит", как бы не так, колба лопнула едва к ней водоструй присосал.
Ссылку дай. Я сам не нашел нормального магазина.
Набор все равно уже оплатил. Хотя бы будет какое-то начало.
Не знаю насчет актуальности цены, но тут http://www.moslabo.ru/production/labpos/kolbykruglodonnye/22/ колбы на 250 со шлифами стоят 100-150 рублей.
Им что, ЗВОНИТЬ нужно что бы что-то купить?
Да я в 3 раза переплачу, лишь бы с людьми не говорить по телефону в 21 веке.
Кстати, нынче таки встречаются обычные плоскодонки, которые отлично держат вакуум. Правда, они стоят дохуя, и с вероятностью 99% плоскодонная колба, доступная анону с двача, таки вакуум держать не будет. Перегонять из плоскодонки в любом случае не стоит.
Ну всякие там бунзенки вакуум держат, но они толстые и редкие. А из плоскодонок без вакуума вполне себе норм перегонять, на мешалку с нагревом поставил и понеслась.
Да, особенности бизнеса в россии, пидорги принципиально не выкладывают цены на сайт и требуют звонить. Видимо чтобы раскрутить лоха на ценник выше прайсового в два раза, а потом дать скидку 5% если заартачится. Или чтобы не надо было объяснять, почему в накладной цена в полтора раза выше цены в прайсе. Пиздец раздражают подобные конторы, никогда у таких не покупаю.
>особенности бизнеса в россии
Няша, ты бы поинтересовался особенностями подобного бизнеса в других странах. В моей милой Америке с заказом всякого хим оборудования ещё веселее фокусы.
Да, только к реальным ценам, по которым эти реагенты отпускаются покупателям, это цены не имеют никакого отношения. А что касается более или менее серьёзного оборудования, то там вообще пиздец бывает. Нужно получать quote, которая будет индивидуально подогнана под тебя.
>пользуются теорией ВС
Ты где таких кретинов нашёл?
Укороченными таблицами только в школах пользуются, не?
Вы видите копию треда, сохраненную 23 февраля 2017 года.
Можете попробовать обновить страницу, чтобы увидеть актуальную версию.
Скачать тред: только с превью, с превью и прикрепленными файлами.
Второй вариант может долго скачиваться. Файлы будут только в живых или недавно утонувших тредах. Подробнее
Если вам полезен архив М.Двача, пожертвуйте на оплату сервера.